Nội dung toàn văn Tiêu chuẩn quốc gia TCVN 11679:2016 (ISO 13969:2003) về Sữa và sản phẩm sữa - Hướng dẫn mô tả chuẩn các phép thử chất ức chế vi khuẩn
TIÊU CHUẨN QUỐC GIA
TCVN 11679:2016
ISO 13969:2003
SỮA VÀ SẢN PHẨM SỮA - HƯỚNG DẪN MÔ TẢ CHUẨN CÁC PHÉP THỬ CHẤT ỨC CHẾ VI KHUẨN
Milk and milk products - Guidelines for a standardized description of microbial inhibitor tests
Lời nói đầu![]()
TCVN 11679:2016 hoàn toàn tương đương với ISO 13969:2003;
TCVN 11679:2016 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F12 Sữa và sản phẩm sữa biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
Lời giới thiệu
Các thông số nêu trong tiêu chuẩn này có thể không cần phải đánh giá đầy đủ cho mỗi phép thử, mà tùy thuộc vào:
a) lĩnh vực ứng dụng của phép thử được nghiên cứu (ví dụ: phương pháp sàng lọc hoặc phương pháp chuẩn, loại sữa, ví dụ sữa của các loài động vật hoặc sữa nguyên liệu/sữa đã xử lý nhiệt),
b) thông tin cần thiết [ví dụ: giới thiệu một chất mới với giới hạn dư lượng tối đa (MRL) cố định], và
c) mô hình phát hiện (ví dụ: độ nhạy của vi sinh vật thử nghiệm đối với một dải rộng hay hẹp của các hợp chất kháng khuẩn).
Như vậy "các thuật ngữ tham chiếu" giữa nhà sản xuất và người sử dụng một phép thử nhất định phải được thống nhất trong nội dung của các hướng dẫn này, ví dụ, những khía cạnh không liên quan đến lĩnh vực dự định áp dụng.
Một bất lợi chung liên quan đến việc diễn giải các phép thử chất ức chế vi khuẩn là chúng thường được đánh giá theo cách chủ quan và đơn giản, nghĩa là nghi ngờ âm tính và dương tính bằng cách so sánh với mẫu kiểm chứng dương tính và/hoặc âm tính.
Trong các trường hợp môi trường có chứa chất chỉ thị, kiểu thay đổi màu sắc có thể phụ thuộc vào sự có mặt loại kháng khuẩn. Điều này đôi khi gây khó khăn cho việc phân biệt rõ ràng giữa các kết quả dương tính và âm tính. Việc diễn giải phép thử theo vài bước cũng có nghĩa là các thay đổi nhỏ hoặc biến màu nhẹ, có thể là quan trọng trong một chương trình đánh giá xác nhận, cần được thực nghiệm.
SỮA VÀ SẢN PHẨM SỮA - HƯỚNG DẪN MÔ TẢ CHUẨN CÁC PHÉP THỬ CHẤT ỨC CHẾ VI KHUẨN
Milk and milk products - Guidelines for a standardized description of microbial inhibitor tests
1 Phạm vi áp dụng
Tiêu chuẩn này đưa ra hướng dẫn để mô tả chuẩn các phép thử chất ức chế vi khuẩn đối với sữa và sản phẩm sữa. Tiêu chuẩn này nhằm đưa ra khuôn khổ và cơ sở cho việc đánh giá/xác nhận các phép thử chất ức chế vi khuẩn, cho phép so sánh các dữ liệu thu được từ các phép thử và các nghiên cứu thực nghiệm khác nhau.
2 Thuật ngữ và định nghĩa
Trong tiêu chuẩn này sử dụng các thuật ngữ và định nghĩa sau đây.
2.1 Dương tính giả (false positives)
Tỷ lệ phần trăm các kết quả dương tính khi thử nghiệm các mẫu âm tính
2.2 Âm tính giả (false negatives)
Tỷ lệ phần trăm các kết quả âm tính ở mức phát hiện công bố.
2.3 Giới hạn phát hiện (limit of detection)
Mức nồng độ mà tại đó phát hiện mẫu thử với một tỷ lệ phần trăm xác định.
VÍ DỤ: 95% cùng với mức tin cậy tương ứng.
3 Thông tin cần thiết từ người xây dựng/nhà sản xuất
3.1 Phương pháp luận
Người xây dựng hoặc nhà sản xuất bộ kit thử cần cung cấp thông tin liên quan đến phương pháp bằng cách đề cập đến những vấn đề sau đây:
a) mô tả phương pháp;
b) nguyên tắc của phương pháp;
c) thiết kế kỹ thuật của quy trình (ví dụ: mức độ tự động hóa, xử lý dữ liệu);
d) đánh giá kết quả thử nghiệm (ví dụ: cho điểm, dùng thang đo và xác định "âm tính" hoặc "dương tính");
e) dung lượng (ví dụ: lượng mẫu);
f) các yêu cầu cụ thể về lấy mẫu, bảo quản và thử nghiệm;
g) quy trình với mục đích đảm bảo chất lượng của người xây dựng/nhà sản xuất bộ kít thử;
h) lĩnh vực ứng dụng liên quan
1) việc dự kiến sử dụng phép thử (ví dụ: sàng lọc hay khẳng định), và
2) chất hoặc nền mẫu (ví dụ: sữa bò hoặc sữa của các động vật khác, sữa bột hay các loại thực phẩm khác).
3.2 Yêu cầu vận hành
Cần quy định các thông tin sau đây liên quan đến các yêu cầu vận hành:
a) các yêu cầu về kinh nghiệm và đào tạo cho người sử dụng;
b) các yêu cầu về an toàn và dịch vụ phòng thử nghiệm đặc biệt (ví dụ: nguồn điện, phòng thử nghiệm S1, xử lý chất thải và mức nồng độ tối đa);
c) các yêu cầu về kiểm soát chất lượng của nhà sản xuất và/hoặc người sử dụng.
3.3 Yêu cầu kỹ thuật của phép thử
Cần có thông tin sau đây liên quan đến các định nghĩa về phép thử:
- Giới hạn phát hiện: xem 2.3.
3.4 Tài liệu
Cần có thông tin sau đây liên quan đến tài liệu:
a) hướng dẫn sử dụng, bao gồm hướng dẫn xử lý sự cố;
b) các nhà cung cấp dụng cụ, thuốc thử, chất chuẩn, dịch vụ kỹ thuật và hỗ trợ khách hàng;
c) tình trạng công nhận chính thức/giới thiệu chung ở các quốc gia cụ thể;
d) có sẵn các tài liệu viện dẫn;
e) có sẵn các tài liệu quốc tế đã được công nhận/đánh giá xác nhận của ISO, IDF và AOAC quốc tế, hoặc những tổ chức khác;
f) có sẵn tài liệu và kinh nghiệm thực tế.
4 Đánh giá các thuộc tính của phép thử chất ức chế vi khuẩn
4.1 Yêu cầu chung
Việc đánh giá xác nhận phương pháp cần thực hiện trong các điều kiện được kiểm soát, nghĩa là dựa trên các mẫu thử nghiệm xác định. Ảnh hưởng của các điều kiện cụ thể được nêu trong 4.3.6.
4.2 Điều kiện tiên quyết
4.2.1 Sữa không chứa các chất kháng khuẩn (“mẫu âm tính”)
Bò cung cấp "mẫu âm tính" phải đáp ứng các yêu cầu sau đây. Tuy nhiên, nếu phép thử được áp dụng cho sữa không phải là sữa bỏ, thì các yêu cầu liên quan đến tình trạng của động vật cần được điều chỉnh cho phù hợp.
a) Tình trạng sức khỏe lâm sàng và cận lâm sàng phải tốt, đặc biệt chú trọng đến tình trạng bầu vú (ít hơn 150 000 tế bào soma trên mililit).
b) Việc điều trị hoặc thức ăn có chứa các chất kháng khuẩn phải bị cấm ít nhất 8 tuần trước khi lấy sữa. Trong trường hợp bò đang phải điều trị, thì không nên lấy sữa trước 60 ngày sau khi đẻ với điều kiện là giai đoạn bò không vắt sữa đã được ít nhất 4 tuần.
c) những con bò đang nuôi con: trên 60 ngày và dưới 200 ngày sau khi sinh, sản xuất hơn 5 kg sữa mỗi ngày.
d) gộp lượng sữa của ít nhất 5 đến 7 con bò để không có biến động về thành phần sữa.
e) số đếm khuẩn lạc phải nhỏ hơn 104 CFU (đơn vị hình thành khuẩn lạc) trên mỗi mililit trước khi bảo quản (đông lạnh sâu, khô lạnh). Sự có mặt của các vi sinh vật sinh β-lactamase phải được lưu ý khi thử nghiệm kháng sinh nhóm β-lactam.
4.2.2 Các chất thử nghiệm
Các chất thử nghiệm được sử dụng trong quy trình cần phải do người xây dựng/nhà sản xuất kít thử đã được công nhận cung cấp, tốt nhất là có giấy chứng nhận phân tích kèm theo quy định kỹ thuật. Nồng độ yêu cầu phải được tính theo axit tự do hoặc các dạng kiểm của thuốc, đã hiệu chính theo độ tinh khiết. Cần đặc biệt chú ý đến độ ổn định/hoạt lực của các chất này.
Tốt nhất là cần thực hiện đánh giá giới hạn phát hiện (4.3.2) sử dụng các chất kháng khuẩn và/hoặc nồng độ mà người xây dựng/nhà sản xuất kít thử khuyến cáo, trừ khi có quy định khác.
4.2.3 Dung môi
Nếu yêu cầu các dung môi đặc biệt hoặc các hóa chất khác để hòa tan các chất, thì cần đảm bảo rằng các dung môi hoặc các hóa chất này trong các mẫu thử không có ảnh hưởng đến kết quả thử nghiệm. Cần hạn chế việc sử dụng các dung môi khác với nước.
4.2.4 Chuẩn bị mẫu thử
4.2.4.1 Yêu cầu chung
Việc chuẩn bị các mẫu thử có thể phát sinh nhiều vấn đề và tốn thời gian cho các phòng thử nghiệm đánh giá thử nghiệm chung. Do đó, có thể sử dụng một hệ thống chuẩn bị mẫu thử tập trung, nhằm cung cấp các mẫu thử ổn định (ví dụ: đông khô) cho các phòng thử nghiệm liên quan.
Để đánh giá quy mô lớn (ví dụ: để có được cơ sở dữ liệu cho một mô tả tổng quát), tất cả các dung dịch pha loãng cần được chuẩn bị theo một mẻ để tránh dao động qua các ngày khác nhau về lượng cân, pha loãng và sai khác về tình trạng của "mẫu âm tính" (4.2.1).
4.2.4.2 Chọn nồng độ
Việc chọn nồng độ cho phép xác định giới hạn phát hiện được nêu trong 4.3.2. Đối với mục đích dự kiến, nếu không có quy định khác, thì nồng độ tìm được giới hạn phát hiện cần được thử nghiệm, cùng với một bước nồng độ cao hơn và hai hoặc ba bước nồng độ thấp hơn giới hạn phát hiện và mẫu âm tính tương ứng. Nhìn chung, nên chia dải nồng độ cho kết quả dương tính từ 50% đến 100% thành ba đến bốn mức khoảng cách bằng nhau (thang logarit và tuyến tính tương ứng) như trong Hình 1.
4.2.4.3 Pha loãng
Cần áp dụng các biện pháp phòng ngừa sau đây khi chuẩn bị dãy pha loãng các chất thử nghiệm.
a) Cần chuẩn bị dãy pha loãng sao cho chỉ có dung dịch pha loãng cuối cùng được chuẩn bị với sữa để tránh liên kết protein.
b) Tỷ lệ dung dịch chất chuẩn được bổ sung vào bước pha loãng sữa cuối cùng gần như nhau cho tất cả các dung dịch pha loãng và ít hơn 1%.
4.2.4.4 Bảo quản
Tốt nhất là bảo quản các mẫu thử nghiệm bằng đông khô, nếu không được quy định bởi người xây dựng/nhà sản xuất kit thử. Quy trình bảo quản sau đây cho thấy có khả thi.
a) Ngay sau khi chuẩn bị của các mẫu thử nghiệm khác nhau, tất cả các dung dịch pha loãng được phân phối vào các ống nghiệm có dung tích thích hợp, để theo tư thế nghiêng và được làm đông lạnh ở -18 °C ± 2 °C.
b) Tiến hành làm đông khô càng nhanh càng tốt và không muộn hơn một tuần sau khi làm đông lạnh sâu. Trong quá trình làm đông khô, nhiệt độ không quá 25 °C.
c) Các ống nghiệm cần được gắn kín ngay sau khi đông khô và được bảo quản nơi tối ở ≤ 6 °C.
d) Các mẫu thử cần được hoàn nguyên trong nước cất. Lượng nước thêm vào cần nhỏ hơn lượng mẫu đã được đông khô là 10% để bù cho lượng chất khô của sữa.
e) Mẫu thử đã hoàn nguyên chỉ được sử dụng trong ngày. Giữ mẫu này trong tủ lạnh giữa các lần sử dụng và loại bỏ vào cuối ngày.
4.2.4.5 Giảm sai sót trong quá trình chuẩn bị
Trong hầu hết các trường hợp, không thể khẳng định được nồng độ kháng khuẩn trong các mẫu thử bằng phương pháp định lượng độc lập. Thực tế để xử lý vấn đề này, nên theo quy trình dưới đây để giảm những sai sót trong quá trình chuẩn bị:
a) Mỗi nhóm 3 đến 5 người cần chuẩn bị các dãy pha loãng riêng và độc lập.
b) Các dãy pha loãng cần được kiểm tra bằng các phép thử chất ức chế vi khuẩn thích hợp hoặc các phương pháp thích hợp khác.
c) Cần chọn các dãy pha loãng cho kết quả thử nghiệm tương tự cho hỗn hợp của các mẫu thử cuối cùng.
4.2.5 Thiết kế thử nghiệm
4.2.5.1 Số lần lặp lại
4.2.5.1.1 Thử nghiệm với số đọc chủ quan
Đối với các phép thử chất ức chế vi khuẩn với số đọc chủ quan và vài kết quả có thể thực hiện được, tất cả các thử nghiệm cần được thực hiện theo các nghiên cứu được mã hóa mù. Số lượng người tham gia, tốt nhất là nhiều hơn một, chịu trách nhiệm về mẫu đã nhận và được mã hóa mà không biết gì về tổ hợp các chất/nồng độ. Các kết quả cần được biểu thị theo phần trăm kết quả dương tính của tổng số lần lặp lại trong mỗi bước nồng độ được đánh giá. Việc tính tỷ lệ phần trăm thường đòi hỏi ít nhất 10 đến 20 lần lặp lại ở mỗi nồng độ được chọn. Độ phân giải số đọc ở mỗi bước nồng độ thử nghiệm tương đương với mức ± 5%, khi thử 20 lần lặp lại. Độ phân giải tương đương với ± 10%, khi thử 10 lần lặp lại.
4.2.5.1.2 Thử nghiệm với số đọc khách quan
Đối với các phép thử chất ức chế vi khuẩn với số đọc khách quan (ví dụ máy đọc ELISA và thang đo), thì thiết kế thử nghiệm không cần thiết nghiên cứu mã hóa mù. Số lần lặp lại phụ thuộc vào độ lặp lại của phương pháp, nhưng phải có ít nhất 3 đến 5 lần lặp lại cho tổ hợp mỗi chất/nồng độ. Nếu yêu cầu độ tin cậy thống kê, thì cần tính số lần lặp lại thích hợp.
Ví dụ, để xác định tỷ lệ âm tính 90% với độ tin cậy 95%, thì cần 60 mẫu cho các số đọc chủ quan và 30 mẫu cho các phép thử diễn giải bằng máy. Nếu không có quy định khác, thì cần sử dụng ít nhất hai lô kít thử khác nhau để đánh giá các thuộc tính khác nhau.
4.2.5.2 Đánh giá dữ liệu thực nghiệm
Đối với việc phân tích dữ liệu, nên thể hiện ở dạng đồ thị, trục x thể hiện nồng độ chất được nghiên cứu và trục y thể hiện phần trăm kết quả dương tính hoặc các giá trị chia độ ("đường đáp ứng liều").
Việc chọn trục x là đường tuyến tính chia độ hoặc lôgarit phụ thuộc vào dải nồng độ thử nghiệm. Nếu dải này bao trùm nồng độ lớn hơn 100 lần, thì thang logarit là thích hợp hơn so với đường tuyến tính. Sử dụng tọa độ này, các điều kiện thử nghiệm khác nhau (ví dụ: lô kít thử nghiệm) để cung cấp các đường đáp ứng liều cho phép so sánh trực quan về ảnh hưởng của các thông số được nghiên cứu.
Đối với đánh giá thống kê, việc xác định độ tin cậy đối với phương pháp được nghiên cứu là bắt buộc. Ví dụ, việc xác định này có thể là giới hạn phát hiện bằng nồng độ mà tại đó 95% các kết quả thử nghiệm là dương tính.
Các giới hạn phát hiện có thể được thể hiện bằng hai cách (xem Hình 1).
a) có giá trị nằm trong hai nồng độ thử nghiệm với giao điểm của đường đáp ứng liều và đường biểu thị "95% kết quả dương tính" (dải nồng độ tính bằng μg/kg), hoặc
b) nồng độ tương ứng với giao điểm của đường đáp ứng liều với đường biểu thị "95% kết quả dương tính".
Đối với mỗi thang đo liên tục, thì tính giá trị trung bình (![]() ) và các độ lệch chuẩn (s) của mỗi nồng độ thử nghiệm, tức là giao điểm của giá trị trung bình trừ 2s (
) và các độ lệch chuẩn (s) của mỗi nồng độ thử nghiệm, tức là giao điểm của giá trị trung bình trừ 2s (![]() -2s) hoặc giá trị trung bình cộng với 2s (
-2s) hoặc giá trị trung bình cộng với 2s (![]() + 2s), phụ thuộc vào độ đáp ứng có tỷ lệ nghịch với nồng độ hay không. Giá trị trên trục y được hiểu là dương tính, tương ứng với giới hạn phát hiện.
+ 2s), phụ thuộc vào độ đáp ứng có tỷ lệ nghịch với nồng độ hay không. Giá trị trên trục y được hiểu là dương tính, tương ứng với giới hạn phát hiện.
Cần lưu ý rằng các giới hạn phát hiện ước tính phụ thuộc vào mức độ nhất định của các nồng độ được thử nghiệm.
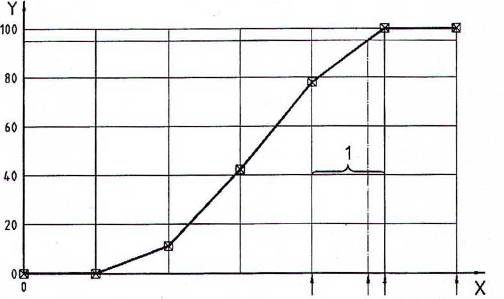
CHÚ DẪN |
|
X hàm lượng chất kháng khuẩn, μg/kg | 3 giới hạn phát hiện |
Y kết quả dương tính,% | 4 mức dư lượng tối đa (MRL) |
1 dải giới hạn phát hiện | 5 1,5 x dương tính dự kiến |
2 dương tính dự kiến |
|
Hình 1 - Mô hình đường đáp ứng liều để xác định giới hạn phát hiện
4.3 Thông số thực nghiệm
4.3.1 Dương tính giả
Thử nghiệm về xác suất dương tính giả bao gồm kiểm tra n lần sữa thử nghiệm âm tính (xem 4.2.1) hoặc các mẫu thử nghiệm âm tính khác thích hợp cho lĩnh vực áp dụng dự kiến. Số lần lặp lại phụ thuộc vào lĩnh vực áp dụng của phép thử.
4.3.2 Giới hạn phát hiện
Việc chọn các hợp chất kháng khuẩn được sử dụng để xác định giới hạn phát hiện phụ thuộc vào công bố của người xây dựng/nhà sản xuất bộ kit thử. Nguyên tắc chuẩn bị mẫu thử được mô tả trong 4.2.4.
Việc chọn các nồng độ để thử nghiệm phải như sau.
a) Ít nhất bốn nồng độ khác nhau cần được kiểm tra giữa mẫu kiểm chứng âm tính và nồng độ dự kiến cho kết quả dương tính.
b) Ngoài ra, cần bao gồm mẫu có nồng độ cao 1,5 lần đến 2 lần so với mẫu cho 100% giá trị dương tính dự kiến.
c) Các nồng độ được chọn cần bao gồm độ nhạy được công bố và nồng độ tương ứng với mọi quy định hiện hành [ví dụ: giá trị giới hạn dư lượng tối đa (MRL)], nếu thích hợp.
d) Các nồng độ được kiểm tra nên càng nhiều càng tốt và theo thực tế nên cách đều trên đường tuyến tính hoặc thang logarit.
e) Mỗi nồng độ cần được kiểm tra sử dụng 10 đến 20 lần lặp lại và thiết kế thử nghiệm cần được thực hiện theo nghiên cứu được mã hóa mù như trong 4.2.5.1.1 đối với các số đọc chủ quan.
f) Đối với các phép thử được diễn giải kết quả trên máy và các kết quả biều thị bằng giá trị số, thì cần ít nhất 3 đến 5 lần lặp lại.
Phần trăm các kết quả dương tính thu được hoặc ở mức công bố giới hạn phát hiện hoặc ở mức "yêu cầu thị trường" (ví dụ: các MRL) của các chất kháng khuẩn liên quan có ý nghĩa quan trọng thực tiễn. Tốt nhất, các thông số này nên được đưa ra dưới dạng đồ thị. Các ví dụ được thể hiện trong Hình 2 đến Hình 4.
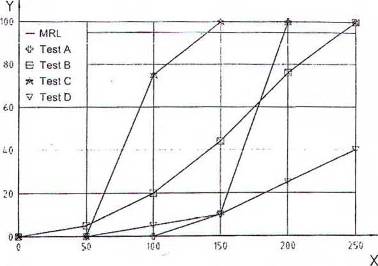
Hình 2 và Hình 3 là một chiều trong đó giới hạn phát hiện của một chất được chứng minh bằng các phép thử khác nhau hoặc các chất khác nhau bằng một phép thử đối với yêu cầu (ví dụ: khái niệm MRL).
CHÚ DẪN
X hàm lượng chất kháng khuẩn, μg/kg
Y kết quả dương tính, %
CHÚ THÍCH: n = 20 (10) cho mỗi nồng độ và kít thử.
Hình 2 - Phát hiện một chất kháng khuẩn bằng các phép thử khác nhau
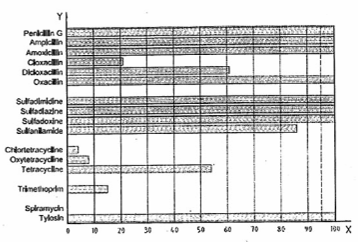
CHÚ DẪN:
X kết quả dương tính, %
Y chất kháng khuẩn
CHÚ THÍCH: Phần trăm kết quả dương tính ở mức MRL, n ≥ 20 (10) cho mỗi chất và nồng độ MRL.
Hình 3 - Mô hình phát hiện các chất kháng khuẩn khác nhau bằng một phép thử
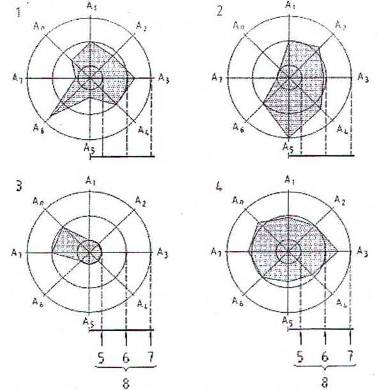
CHÚ DẪN:
1 phép thử 1 2 phép thử 2 3 phép thử 3 4 phép thử 4 | 5 ≥ 10 MRL 6 1 MRL 7 ≤ 0,1 MRL 8 Giới hạn phát hiện |
CHÚ THÍCH: Giới hạn phát hiện được biểu thị bằng nồng độ x lần MRL.
Hình 4 - Mô hình phát hiện (vùng hiện màu) các phép thử chất ức chế vi khuẩn khác nhau đối với các chất kháng khuẩn A1, A2,…An
Các ví dụ nêu trong Hình 4 là mô hình phát hiện của các phép thử khác nhau (trong ví dụ này có bốn phép thử) liên quan đến một số kháng sinh (trong ví dụ này có n vi khuẩn). Trục giới hạn phát hiện đã được chuẩn hóa liên quan đến các MRL của các chất kháng khuẩn (nồng độ x lần MRL). Thang đo phụ thuộc vào dải biến thiên là quan trọng. Trong ví dụ này, thang chuẩn hóa bao gồm dải từ ≤ 0,1 MRL đến ≥ 10 MRL.
Phép thử nghiệm lý tưởng cần phát hiện 1 MRL của tất cả các chất kháng khuẩn liên quan, tương ứng với các vòng trung tâm của Hình 4. Việc phát hiện một chất kháng khuẩn nhạy hơn là có liên quan đến yêu cầu của MRL, tiếp nữa là khoảng cách từ trung tâm thang đo MRL đã chuẩn hóa và ngược lại. Hình ảnh của mô hình phát hiện của phép thử thu được bằng cách kết nối với các giới hạn phát hiện đã được chuẩn hóa của các chất kháng khuẩn. Các mô hình phát hiện các phép thử khác nhau có thể dễ dàng so sánh. Việc xác định các giới hạn phát hiện của các phép thử khác nhau/các hợp chất kháng khuẩn cần được chỉ ra theo như dữ liệu có sẵn.
4.3.3 Sự dao động của giới hạn phát hiện giữa các lô hàng
Mục tiêu của việc kiểm tra này là để biết được sự dao động của các độ đáp ứng thử nghiệm do bị ảnh hưởng bởi các yếu tố sản xuất khác nhau của kít thử (ví dụ: tác động của chất chỉ thị, các chất dinh dưỡng, vi sinh vật thử nghiệm). Điều này có thể được dự kiến rằng sự dao động của tất cả những yếu tố này có thể tăng theo khoảng thời gian tăng dần giữa các lô sản xuất. Do đó, các lô thử nghiệm nên có thời gian sản xuất càng xa nhau càng tốt (ví dụ: một hoặc hai lần mỗi năm).
Việc kiểm tra và đánh giá được thực hiện theo 4.2.5. Việc xác định thuật ngữ "lô hàng" chủ yếu dựa vào những thông tin được cung cấp bởi nhà sản xuất. Hình 5 minh họa thực nghiệm trong đó các giới hạn phát hiện của chất kháng khuẩn đã được thử nghiệm trên mười một lô kít thử khác nhau trong khoảng thời gian hơn nửa năm. Trong ví dụ này, các giới hạn phát hiện dao động trong khoảng 8 μg/kg đến 10 μg/kg.
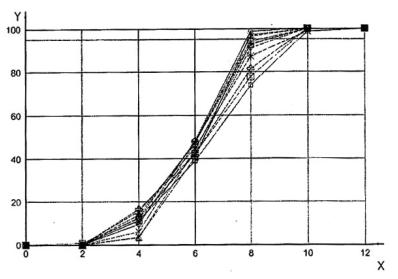
CHÚ DẪN
X hàm lượng chất kháng khuẩn, μg/kg
Y % kết quả dương tính
Hình 5 - Độ tái lập giữa mười một lô kit thử - Một vi khuẩn
4.3.4 Dao động của các giới hạn phát hiện trong lô hàng
Quy trình kiểm tra tương tự như quy trình trong 4.3.3, trừ các bộ kít thử từ một lô hàng được kiểm tra 3 đến 5 lần trong một khoảng thời gian ngắn.
4.3.5 Thời hạn sử dụng của các bộ kit thử
Để kiểm tra sự dao động của phản ứng thử nghiệm trong suốt thời hạn sử dụng đã được công bố, chọn các chất thử nghiệm theo quy trình trong 4.2. Số lần lặp lại và đánh giá theo quy trình trong 4.2.5. Cần thực hiện kiểm tra ít nhất ba lần (ban đầu ở mức 90% và ở cuối hạn sử dụng đã được công bố). Các điều kiện bảo quản (ví dụ: nhiệt độ, thời gian), phải tuân thủ hướng dẫn của người xây dựng/nhà sản xuất bộ kít thử.
4.3.6 Độ nhạy với nhiễu (độ chắc chắn)
4.3.6.1 Yêu cầu chung
Cần tiến hành nghiên cứu độ nhạy với chất gây nhiễu của bộ kít thử trong quá trình nghiên cứu theo các lưu ý sơ bộ trong phần giới thiệu. Nghiên cứu này cũng có thể bao gồm mọi ảnh hưởng hợp lực/đối kháng của tổ hợp các hoạt chất.
4.3.6.2 Quy trình thử nghiệm
Do các mẫu kiểm chứng (âm tính hay dương tính) có thể phản ứng khác nhau với các mẫu thử nghiệm có chứa hợp chất kháng khuẩn khác so với các mẫu kiểm chứng, các yếu tố gây nhiễu tiềm năng trong quá trình thử nghiệm (ví dụ thuốc thử, các điều kiện ủ hoặc lượng mẫu) cần được kiểm tra. Đối với nghiên cứu này, cần chuẩn bị các mẫu thử với tổ hợp các chất/nồng độ được chọn theo 4.2. Phương pháp thực nghiệm, kể cả một số sai lệch xác định so với quy trình thử nghiệm đúng cần được kiểm tra, tùy thuộc vào kinh nghiệm của hội đồng đánh giá.
4.3.6.3 Thành phần/đặc tính của mẫu
Kết quả của các phép thử chất ức chế vi khuẩn có thể bị ảnh hưởng bởi một số yếu tố liên quan đến thành phần/đặc tính của mẫu. Các yếu tố, ví dụ: chất lượng vi khuẩn, lượng tế bào soma, hàm lượng chất béo và chất lượng của nó, giá trị pH, loài động vật và trạng thái cho sữa của các động vật như sữa non và dư lượng của các chất tẩy rửa hoặc quá trình xử lý sữa như quy trình gia nhiệt hoặc sấy khô.
Trong việc kiểm tra này, có tính đến những hạn chế do người xây dựng/nhà sản xuất kít thử quy định, hai vấn đề sau đây cần được xem xét.
a) Các yếu tố như vậy có dẫn đến kết quả dương tính “giả”, ví dụ hàm lượng lysozyme tăng cao trong sữa non? (Được kiểm tra với sữa không có kháng sinh.)
b) Các yếu tố như vậy có dẫn đến kết quả âm tính “giả”, ví dụ ảnh hưởng bị che khuất do vi sinh vật sinh β-lactamase ? (Được kiểm tra với sữa thêm chuẩn.)
Để kiểm tra ảnh hưởng của số đếm tế bào soma cao trong mẫu, tốt nhất nên sử dụng các mẫu sữa từ bò bị nhiễm "tự nhiên" chưa được điều trị bằng các chất kháng khuẩn.
4.3.6.4 Bảo quản mẫu
Các mẫu thử cần được kiểm tra các chất ức chế có thể được bảo quản bằng cách bổ sung hóa chất (ví dụ axit boric) hoặc bằng cách làm đông lạnh sâu. Cần kiểm tra các kết quả dương tính “giả” và âm tính “giả” như trong 4.3.6.3.
Nếu chưa có công bố của người xây dựng/nhà sản xuất, ảnh hưởng của hóa chất bảo quản phải kiểm tra không chỉ ở nồng độ quy định mà còn ở nồng độ thấp hơn và cao hơn để ước tính độ nhạy của phép thử được nghiên cứu về nồng độ chất bảo quản. Các mẫu thử phải được phân tích trước khi bảo quản, sau khi bảo quản và lưu trữ. Vì việc bổ sung các chất bảo quản có thể làm thay đổi thời gian ủ yêu cầu của phép thử, nên các mẫu kiểm chứng cần được bảo quản tương ứng.
Kiểm tra hiệu quả của việc bảo quản mẫu lâu dài (ví dụ: bằng cách làm lạnh sâu) gặp phải những khó khăn sau đây:
a) hạn sử dụng của các bộ kít thử có thể hạn chế thời gian bảo quản mà có thể cần được kiểm tra, nếu các lô kit thử như nhau được sử dụng trong toàn bộ thời gian bảo quản; hoặc là
b) sự thay đổi giữa các lô kít thử có thể làm tăng sự thay đổi trong các kết quả, nếu các lô kít thử khác nhau được sử dụng trong suốt thời gian bảo quản mẫu.
4.3.7 Phát hiện các chất phát sinh
Điều kiện tiên quyết đối với việc phân tích các chất phát sinh là các thử nghiệm điều trị với một số bò sử dụng các loại thuốc thực tế bán trên thị trường để sử dụng tại trang trại và định lượng chất được áp dụng trong các mẫu sữa bằng phương pháp chuẩn định lượng. Nếu có sẵn, sử dụng chất chuẩn từ các tổ chức được công nhận (ví dụ BCR1)). Cần chuẩn bị các mẫu thử với nồng độ theo 4.2.4.2 bằng cách pha loãng thích hợp các mẫu sữa có nồng độ đã được xác nhận.
4.3.8 Các nghiên cứu hợp tác
Đối với các nghiên cứu hợp tác, cần chuẩn bị các mẫu thử trong một phòng thử nghiệm theo 4.2.4. Các mẫu thử phải được vận chuyển cùng với các kít thử, trong điều kiện thích hợp, có ít nhất 8 phòng thử nghiệm tham gia trong trường hợp phân tích định lượng và ít nhất 15 phòng thử nghiệm trong trường hợp phân tích định tính.
Việc chọn chất hoặc tổ hợp nồng độ thích hợp cần theo quy trình trong 4.2. Các mẫu thử phải được mã hóa và mỗi chất hoặc tổ hợp nồng độ cần được phân tích trong mỗi phòng thử nghiệm tham gia ít nhất 10 đến 20 lần (đọc trực quan), hoặc 3 đến 5 lần (thử nghiệm với thang đo) cho mỗi lô kít thử nghiệm. Quy trình thực nghiệm nghiêm ngặt là bắt buộc.
5 Đánh giá các thông số đo
5.1 Khả năng áp dụng đối với mục đích sử dụng
Ý kiến chuyên gia về khả năng áp dụng đối với mục đích sử dụng như sau.
a) Các thông số đo được của phép thử chất ức chế vi khuẩn cần kiểm tra, có thể thu được từ các nghiên cứu khác nhau được thực hiện vào những dịp khác nhau, cần được thu thập theo hình thức bảng.
b) Thông tin nêu trong phần nội dung (dạng bảng) tạo cơ sở cho phần thông tin thứ hai bao gồm quan điểm của chuyên gia, xếp hạng và đánh giá thông tin được đưa ra có liên quan đặc biệt đến lĩnh vực áp dụng của phép thử được tuyên bố/đề nghị.
c) Xem xét thực tế là việc xây dựng các thuộc tính khác nhau cần nhiều hoặc ít thời gian hơn, đặc biệt là nếu thời gian bảo quản được nghiên cứu (ví dụ: xác định thời hạn sử dụng), báo cáo bao gồm xếp hạng các thuộc tính được xây dựng cần được đưa ra trong các phần theo lịch trình nhất định.
Các chuyên gia cần đánh giá liên tục các dữ liệu hoặc thông tin mới sẵn có.
5.2 Báo cáo
Để báo cáo liên tục, các nội dung cần theo thứ tự sau.
Phần 1
1) giới hạn phát hiện (4.3.2);
2) dao động trong lô hàng (4.3.4)
3) dương tính giả (4.3.1).
Phần 2
1) độ nhạy với nhiễu (độ chắc chắn) (4.3.6);
2) phát hiện các chất phát sinh (4.3.7).
Phần 3
1) sự dao động giữa các lô hàng (4.3.3);
2) thời hạn sử dụng (4.3.5);
3) nghiên cứu cộng tác (4.3.8).
1) BCR là Văn phòng Cộng đồng Chuẩn của Hội đồng Châu Âu. Các chất chuẩn có bán sẵn từ Viện chất chuẩn và đo lường (IRMM), Ban quản lý đơn vị chất chuẩn (MRM), Retiesweg, B 2440 Geel, Bỉ. Thông tin này đưa ra để thuận tiện cho người sử dụng tiêu chuẩn này và không ấn định phải sử dụng chúng.