Quyết định 1098/QĐ-BYT hướng dẫn quốc gia về xét nghiệm huyết thanh học HIV 2013 đã được thay thế bởi Quyết định 2674/QĐ-BYT 2018 hướng dẫn quốc gia xét nghiệm HIV và được áp dụng kể từ ngày 27/04/2018.
Nội dung toàn văn Quyết định 1098/QĐ-BYT hướng dẫn quốc gia về xét nghiệm huyết thanh học HIV 2013
|
BỘ Y TẾ |
CỘNG HÒA XÃ
HỘI CHỦ NGHĨA VIỆT NAM |
|
Số: 1098/QĐ-BYT |
Hà Nội, ngày 04 tháng 4 năm 2013 |
QUYẾT ĐỊNH
VỀ VIỆC BAN HÀNH HƯỚNG DẪN QUỐC GIA VỀ XÉT NGHIỆM HUYẾT THANH HỌC HIV
BỘ TRƯỞNG BỘ Y TẾ
Căn cứ Nghị định số 63/2012/NĐ-CP ngày 31 tháng 8 năm 2012 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Theo đề nghị của Cục trưởng Cục Phòng, chống HIV/AIDS,
QUYẾT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này “Hướng dẫn quốc gia về xét nghiệm huyết thanh học HIV”.
Điều 2. Quyết định này có hiệu lực kể từ ngày ký, ban hành.
Điều 3. Các ông, bà: Chánh Văn phòng Bộ, Cục trưởng, Vụ trưởng, Tổng cục trưởng các Vụ, Cục, Tổng cục, Thủ trưởng các đơn vị trực thuộc Bộ Y tế, Giám đốc Sở Y tế các tỉnh/thành phố trực thuộc Trung ương, Thủ trưởng các đơn vị liên quan chịu trách nhiệm thi hành Quyết định này./.
|
Nơi nhận: |
KT. BỘ
TRƯỞNG |
HƯỚNG DẪN
QUỐC GIA VỀ XÉT NGHIỆM HUYẾT THANH HỌC HIV
(Ban
hành kèm theo Quyết định số 1098/QĐ-BYT ngày 04 tháng 4 năm 2013 của Bộ trưởng
Bộ Y tế)
Chương I
XÉT NGHIỆM HIV Ở VIỆT NAM
I. MỤC ĐÍCH XÉT NGHIỆM HIV
1. An toàn truyền máu và cấy ghép mô, nội tạng: xét nghiệm sàng lọc HIV để đảm bảo an toàn truyền máu và các chế phẩm của máu, cấy ghép mô và nội tạng, cho tinh dịch, trứng, phôi (sau đây gọi chung là an toàn truyền máu).
2. Giám sát dịch tễ HIV/AIDS: xác định tỷ lệ nhiễm HIV trong một số nhóm quần thể nhất định theo thời gian và địa điểm nhằm theo dõi sự phân bố, chiều hướng phát triển của dịch nhằm cung cấp thông tin cho việc lập kế hoạch, dự phòng, khống chế và đánh giá hiệu quả các biện pháp phòng, chống HIV/AIDS.
3. Chẩn đoán nhiễm HIV: xác định tình trạng nhiễm HIV của người được làm xét nghiệm.
4. Dùng cho các mục đích nghiên cứu.
II. NGUYÊN TẮC XÉT NGHIỆM HIV
1. Đảm bảo tính bí mật, tự nguyện.
2. Được tư vấn trước và sau xét nghiệm.
3. Tuân thủ chiến lược và phương cách xét nghiệm.
4. Đảm bảo chất lượng xét nghiệm.
III. CÁC CHIẾN LƯỢC XÉT NGHIỆM
Xét nghiệm HIV được tiến hành theo những chiến lược khác nhau tùy thuộc vào mục đích xét nghiệm, tỷ lệ hiện nhiễm HIV của quần thể xét nghiệm.
1. Chiến lược I (áp dụng cho an toàn truyền máu): mẫu được coi là dương tính với kháng thể HIV khi mẫu đó có phản ứng với một xét nghiệm bằng sinh phẩm (sau đây được ký hiệu là SP) có độ nhạy cao. Trong an toàn truyền máu, cấy ghép mô tạng và thụ tinh nhân tạo, những túi máu, sản phẩm máu hoặc mô, bộ phận cơ thể phải loại bỏ nếu có kết quả xét nghiệm dương tính hoặc nghi ngờ.
2. Chiến lược II (áp dụng cho giám sát dịch tễ): mẫu được coi là dương tính với chiến lược II khi mẫu đó có phản ứng với cả hai loại sinh phẩm có nguyên lý hoặc chuẩn bị kháng nguyên khác nhau, sinh phẩm thứ nhất (SP1) phải có độ nhạy cao, sinh phẩm thứ hai (SP2) có độ đặc hiệu cao.
2.1. Kết quả xét nghiệm với sinh phẩm thứ nhất không có phản ứng, kết luận mẫu âm tính với kháng thể HIV.
2.2. Kết quả xét nghiệm với sinh phẩm thứ nhất cho phản ứng (SP1+), tiếp tục thực hiện xét nghiệm với sinh phẩm thứ hai.
- Kết quả xét nghiệm bằng sinh phẩm thứ hai cho phản ứng (SP1+, SP2+), kết luận mẫu dương tính với kháng thể HIV.
- Kết quả xét nghiệm bằng sinh phẩm thứ hai không có phản ứng (SP1+, SP2-), kết luận mẫu âm tính với kháng thể HIV.
2.3. Kết quả xét nghiệm này chỉ dùng cho mục đích giám sát dịch tễ không thông báo cho người được làm xét nghiệm.
2.4. Lưu ý: chỉ được thông báo kết quả cho người được làm xét nghiệm khi tiếp tục thực hiện xét nghiệm bằng sinh phẩm thứ ba (SP3) theo quy định của chiến lược III.
3. Chiến lược III (áp dụng cho xét nghiệm chẩn đoán nhiễm HIV): mẫu được coi là dương tính với chiến lược III khi mẫu đó có phản ứng với cả ba loại sinh phẩm có nguyên lý hoặc chuẩn bị kháng nguyên khác nhau. Sinh phẩm thứ nhất (SP1) dùng để sàng lọc có độ nhạy cao, các sinh phẩm tiếp theo (SP2, SP3) để khẳng định có độ đặc hiệu cao.
3.1. Kết quả xét nghiệm với sinh phẩm thứ nhất không có phản ứng, kết luận mẫu âm tính với kháng thể HIV.
3.2. Kết quả xét nghiệm với sinh phẩm thứ nhất cho phản ứng (SP1+), tiếp tục thực hiện xét nghiệm với sinh phẩm thứ hai (SP2).
a) Kết quả xét nghiệm bằng sinh phẩm thứ hai cho phản ứng (SP1+, SP2+), thì tiếp tục thực hiện với sinh phẩm thứ ba (SP3).
- Kết quả xét nghiệm với sinh phẩm thứ ba cho phản ứng (SP1+, SP2+, SP3+), kết luận mẫu dương tính với kháng thể HIV và được phép trả lời kết quả cho người được làm xét nghiệm.
- Kết quả xét nghiệm với sinh phẩm thứ ba không cho phản ứng (SP1+, SP2+, SP3-), kết luận mẫu không xác định, yêu cầu lấy mẫu xét nghiệm lại sau 14 ngày.
b) Kết quả xét nghiệm bằng sinh phẩm thứ hai không cho phản ứng (SP1+, SP2-), thực hiện lại xét nghiệm với cả sinh phẩm thứ nhất (SP1) và thứ hai (SP2) để kiểm tra loại trừ sai sót kỹ thuật.
b1. Nếu kết quả xét nghiệm với cả hai sinh phẩm không cho phản ứng (SP1-, SP2-), kết luận mẫu âm tính với kháng thể HIV;
b2. Nếu kết quả xét nghiệm (SP1+, SP2+) hoặc (SP1+, SP2-) thực hiện tiếp xét nghiệm với sinh phẩm thứ ba (SP3), kết quả cả 3 lần làm xét nghiệm sẽ được phân tích và biện luận như sau:
+ Kết quả xét nghiệm (SP1+, SP2+, SP3+), kết luận mẫu dương tính với kháng thể HIV.
+ Kết quả xét nghiệm (SP1+, SP2+, SP3-) hoặc (SP1+, SP2-, SP3+), kết luận mẫu không xác định, yêu cầu lấy mẫu xét nghiệm lại sau 14 ngày.
+ Kết quả xét nghiệm (SP1+, SP2-, SP3-) và người được làm xét nghiệm không có yếu tố nguy cơ lây nhiễm HIV có thể kết luận là mẫu âm tính với kháng thể HIV; nếu người được làm xét nghiệm có yếu tố nguy cơ lây nhiễm HIV, kết luận mẫu không xác định và yêu cầu lấy mẫu xét nghiệm lại sau 14 ngày; trường hợp người được làm xét nghiệm không có yếu tố nguy cơ lây nhiễm HIV nhưng nếu SP1 là sinh phẩm xét nghiệm phát hiện cả kháng nguyên và kháng thể trong khi SP2 và SP3 là sinh phẩm chỉ phát hiện kháng thể thì yêu cầu lấy mẫu xét nghiệm lại sau 14 ngày.
3.3. Trong các trường hợp kết quả xét nghiệm không xác định, đề nghị lấy máu xét nghiệm lại lần 2 sau 14 ngày và nếu kết quả xét nghiệm sau 14 ngày vẫn tiếp tục không xác định thì phân tích và biện luận như sau:
- Không có sự thay đổi hoặc giảm mức độ phản ứng với cùng loại sinh phẩm đã được sử dụng trong 2 lần xét nghiệm, kết luận mẫu âm tính với kháng thể HIV.
- Có sự gia tăng mức độ phản ứng với cùng loại sinh phẩm đã được sử dụng trong 2 lần xét nghiệm, yêu cầu lấy mẫu làm lại xét nghiệm lần 3 sau 14 ngày
- Các phòng xét nghiệm có thể gửi mẫu không xác định lên phòng xét nghiệm tham chiếu tuyến trên để làm các xét nghiệm khẳng định khác.
3.4. Trong các trường hợp kết quả xét nghiệm lần 3 tiếp tục không xác định, kết luận mẫu âm tính với kháng thể HIV.
IV. THỰC HIỆN XÉT NGHIỆM CHẨN ĐOÁN HIV
1. Phòng xét nghiệm sàng lọc HIV
a) Nếu kết quả xét nghiệm sàng lọc âm tính thì tư vấn và trả lời kết quả cho người được làm xét nghiệm là âm tính với kháng thể HIV.
b) Nếu kết quả xét nghiệm sàng lọc dương tính, mẫu bệnh phẩm cần được gửi lên phòng xét nghiệm khẳng định HIV.
2. Phòng xét nghiệm khẳng định HIV
a) Thực hiện xét nghiệm sàng lọc bằng một loại sinh phẩm và xét nghiệm khẳng định với các mẫu lần đầu có phản ứng theo chiến lược III và trả lời kết quả cho người được làm xét nghiệm hoặc các phòng xét nghiệm gửi mẫu khẳng định.
b) Chỉ những phòng xét nghiệm được Bộ Y tế cấp giấy chứng nhận là phòng xét nghiệm khẳng định HIV mới được phép trả lời kết luận các trường hợp nhiễm HIV.
c) Trường hợp người được làm xét nghiệm lần đầu có kết quả xét nghiệm dương tính với kháng thể HIV nên lấy máu xét nghiệm lại lần 2 để tránh nhầm lẫn trong trường hợp lấy máu lần đầu.
V. PHƯƠNG CÁCH XÉT NGHIỆM HIV
1. Phương cách xét nghiệm: là thứ tự thực hiện các xét nghiệm bằng các sinh phẩm cụ thể đã được lựa chọn.
2. Thứ tự thực hiện xét nghiệm bằng các sinh phẩm được lựa chọn trong một phương cách xét nghiệm cần bảo đảm nguyên tắc: sinh phẩm sàng lọc đầu tiên phải có độ nhạy cao, các sinh phẩm bổ sung phải có độ đặc hiệu cao ưu tiên các sinh phẩm có độ nhậy cao.
Việc xây dựng các phương cách xét nghiệm cần lựa chọn từ các sinh phẩm không hoặc ít có cùng nhược điểm như cùng âm tính giả hoặc cùng dương tính giả.
Lựa chọn một phương cách xét nghiệm tùy thuộc vào: mục đích xét nghiệm; số lượng mẫu; yêu cầu thời gian trả lời kết quả; tỷ lệ nhiễm; điều kiện cụ thể và năng lực thực tế của cơ sở xét nghiệm.
Các sinh phẩm xét nghiệm phải được Bộ Y tế cho phép sử dụng.
VI. SINH PHẨM XÉT NGHIỆM HIV
1. Độ nhạy và độ đặc hiệu là hai yếu tố quan trọng xác định chất lượng của một sinh phẩm xét nghiệm HIV.
2. Sinh phẩm có độ nhạy cao cho kết quả âm tính giả thấp, sinh phẩm có độ nhạy cao thường dùng trong xét nghiệm sàng lọc, đặc biệt trong sàng lọc an toàn truyền máu hoặc cấy ghép mô, nội tạng, cần tuân thủ các quy định chuyên môn trong công tác an toàn truyền máu hoặc được sử dụng trong xét nghiệm sàng lọc ban đầu trong chẩn đoán nhiễm HIV.
3. Một sinh phẩm có độ đặc hiệu cao cho kết quả dương tính giả thấp, sinh phẩm có độ đặc hiệu cao thường dùng trong các xét nghiệm lần thứ 2 và thứ 3 trong chẩn đoán nhiễm HIV.
a) Các sinh phẩm dùng trong xét nghiệm HIV phải có độ nhạy tối thiểu > 99,5% đối với các sinh phẩm xét nghiệm nhanh, 100% với các kỹ thuật ELISA/hóa phát quang/điện hóa phát quang và độ đặc hiệu tối thiểu > 98%. Các tiêu chuẩn này cần dựa theo các đánh giá tiêu chuẩn của các tổ chức Y tế Thế giới, CDC Hoa kỳ hoặc đánh giá của Quốc gia và các đánh giá của các tổ chức có uy tín khác.
b) Trong an toàn truyền máu phải sử dụng các sinh phẩm có độ nhạy cao với mẫu chuyển đổi huyết thanh.
c) Các sinh phẩm phải phát hiện được kháng thể kháng HIV1 và HIV2 trong đó có khả năng phát hiện được tất cả các phân nhóm của HIV-1 trong đó chú ý đến phân nhóm M, N, O.
VII. PHƯƠNG PHÁP XÉT NGHIỆM HIV
Các xét nghiệm phát hiện nhiễm HIV được chia thành các phương pháp chính:
1. Phương pháp gián tiếp: phát hiện sự hiện diện của kháng thể kháng HIV trong máu hoặc các dịch tiết để xác định tình trạng nhiễm HIV ở người lớn và trẻ em trên 18 tháng tuổi.
2. Phương pháp trực tiếp: phát hiện sự hiện diện các thành phần của HIV
a) Phát hiện các axit nucleotit của vi rút:
+ HIV-ADN provirus (có trong tế bào nhiễm).
+ HIV-ARN (vi rút tự do trong huyết tương).
b) Phát hiện kháng nguyên vi rút trong máu (p24).
3. Phương pháp phát hiện đồng thời kháng nguyên và kháng thể.
Chương II
QUẢN LÝ CHẤT LƯỢNG XÉT NGHIỆM HIV
I. TIÊU CHUẨN TRANG THIẾT BỊ, NHÂN LỰC, CƠ SỞ VẬT CHẤT.
Các cơ sở xét nghiệm phải đảm bảo tiêu chuẩn về trang thiết bị, nhân lực, cơ sở vật chất theo quy định của Hướng dẫn đảm bảo chất lượng thực hiện kỹ thuật xét nghiệm HIV.
II. ĐẢM BẢO CHẤT LƯỢNG TRONG QUÁ TRÌNH XÉT NGHIỆM
1. Giai đoạn trước xét nghiệm
a) Thu thập mẫu:
- Kiểm tra đối chiếu để lấy mẫu đúng người bệnh.
- Thu thập đúng và đủ các thông tin về mẫu bệnh phẩm so sánh đối chiếu với phiếu thu thập mẫu gồm có: mã số/tên người được làm xét nghiệm, năm sinh, địa danh lấy mẫu và ngày thu thập mẫu.
- Quy trình lấy mẫu (lấy máu tĩnh mạch hoặc lấy máu đầu ngón tay) đảm bảo phù hợp với yêu cầu của xét nghiệm về loại mẫu, thể tích, chất bảo quản, thời gian và chất lượng.
- Sau khi lấy mẫu các ống nghiệm cần phải được đậy chặt nắp (đối với trường hợp lấy máu tĩnh mạch).
- Sử dụng găng tay và bơm kim tiêm/kim chích riêng cho từng người được làm xét nghiệm thao tác an toàn tránh lây nhiễm chéo giữa các mẫu bệnh phẩm và lây nhiễm cho người được làm xét nghiệm và nhân viên y tế.
b) Bảo quản và lưu trữ mẫu
- Mẫu máu phải tách huyết thanh hoặc huyết tương trong vòng 24 giờ. Huyết thanh và huyết tương có thể bảo quản ở nhiệt độ từ 4-8oC tối đa 7 ngày, nếu không xét nghiệm trong vòng 7 ngày mẫu phải được bảo quản ở tối thiểu âm 20oC hoặc lạnh hơn và không tan đông quá 3 lần.
- Ghi chép và lưu trữ sổ theo dõi mẫu theo quy định.
c) Đóng gói và vận chuyển mẫu
- Đóng gói và vận chuyển phải tuân thủ nguyên tắc an toàn sinh học theo Thông tư số 43/2011/TT-BYT ngày 05/12/2011 của Bộ Y tế về Quy định chế độ quản lý mẫu bệnh phẩm bệnh truyền nhiễm và hướng dẫn tại phụ lục 1 của Quyết định này.
- Gửi mẫu kèm 02 bản danh sách mẫu và phiếu gửi mẫu xét nghiệm HIV tới cơ sở xét nghiệm theo quy định.
- Trường hợp vận chuyển trong nội bộ đơn vị thì mẫu cũng cần được để trong hộp an toàn có nắp đậy.
d) Tiếp nhận mẫu
- Phòng xét nghiệm cần có tiêu chuẩn chấp nhận và từ chối nhận mẫu.
- Kiểm tra quy cách đóng gói mẫu, chất lượng mẫu theo tiêu chuẩn: thể tích; nhiệt độ vận chuyển; mẫu có bị tán huyết, nhiễm khuẩn không; chất chống đông sử dụng.
- Đối chiếu thông tin trên ống mẫu với phiếu gửi mẫu khi nhận mẫu.
+ Trường hợp thiếu các thông tin trên phiếu gửi mẫu phải thông báo cho nơi gửi mẫu để bổ sung thông tin và rút kinh nghiệm cho các lần sau.
+ Trường hợp mẫu không đạt chất lượng phòng xét nghiệm từ chối nhận mẫu xét nghiệm và yêu cầu lấy lại mẫu.
- Ghi chép đầy đủ các thông tin vào sổ nhận mẫu, ký xác nhận vào bản danh sách gửi mẫu và lưu giữ theo quy định.
- Thông báo thời gian trả kết quả cho đơn vị gửi mẫu.
2. Giai đoạn trong xét nghiệm
a) Chuẩn bị mẫu
- Lập sơ đồ mẫu trước khi xét nghiệm và sắp xếp các mẫu theo đúng sơ đồ để tránh nhầm lẫn.
- Trên phiếu sơ đồ mẫu xét nghiệm cần ghi đầy đủ các thông tin: tên sinh phẩm, số lô, hạn sử dụng, ngày thực hiện xét nghiệm và người thực hiện xét nghiệm.
b) Sinh phẩm và vật tư tiêu hao
- Sinh phẩm sử dụng trong xét nghiệm HIV:
+ Sinh phẩm phải được Bộ Y tế cho phép sử dụng; lựa chọn những sinh phẩm đáng tin cậy và có tiêu chuẩn kỹ thuật phù hợp cho xét nghiệm sàng lọc hoặc xét nghiệm bổ sung.
+ Chỉ sử dụng những sinh phẩm còn trong hạn sử dụng: hạn ghi trên hộp sinh phẩm và hạn sau khi mở hoặc đã pha các chất thử theo quy định của nhà sản xuất.
+ Chỉ được sử dụng sinh phẩm và hóa chất trong một hộp sinh phẩm hoặc cùng lô sản xuất.
+ Nên theo dõi và kiểm tra chất lượng của sinh phẩm khi nhận được đợt giao hàng mới hoặc khi thay đổi lô sinh phẩm mới.
+ Kiểm tra các hóa chất trong hộp sinh phẩm trước khi dùng và ngừng sử dụng khi phát hiện dấu hiệu bất thường để xác định nguyên nhân và báo cho nhà cung cấp.
+ Bảo quản sinh phẩm theo hướng dẫn của nhà sản xuất.
- Các vật tư tiêu hao của phòng xét nghiệm phải luôn sẵn có, đúng chủng loại, chất lượng theo yêu cầu.
- Quản lý sinh phẩm và vật tư tiêu hao theo quy định: phải có sổ sách ghi chép, theo dõi số lượng tồn dư để dự trù đủ số lượng theo yêu cầu, tránh hết hạn.
c) Trang thiết bị
- Phòng xét nghiệm phải có đủ các trang thiết bị phù hợp với kỹ thuật thực hiện.
- Quản lý trang thiết bị theo quy định: Lắp đặt và vận hành theo hướng dẫn; Có lý lịch máy (tên; số hiệu; tên nhà sản xuất, phân phối; ngày lắp đặt, vận hành; người quản lý và số điện thoại bảo hành sửa chữa khi cần thiết); Hướng dẫn sử dụng tóm tắt và chi tiết; Nhật ký sử dụng riêng cho từng trang thiết bị, được ghi chép sau mỗi lần sử dụng. Hồ sơ trang thiết bị được lưu giữ đến khi thanh lý.
- Trang thiết bị phải được bảo dưỡng, bảo trì và hiệu chuẩn định kỳ theo quy định.
d) Cơ sở phòng xét nghiệm
- Phòng xét nghiệm phải được thiết kế và bố trí hợp lý đảm bảo đủ không gian làm việc và điều kiện phù hợp với kỹ thuật xét nghiệm HIV và tuân theo các quy định hiện hành của Bộ Y tế.
- Quy định cụ thể ai được phép vào làm việc tại phòng xét nghiệm.
e) Quy trình xét nghiệm
- Phòng xét nghiệm phải xây dựng quy trình thao tác chuẩn (Standar Operating Procedure - SOP) phù hợp với các kỹ thuật đang thực hiện theo đúng hướng dẫn của nhà sản xuất; SOP phải chính xác, ngắn gọn, dễ hiểu và đầy đủ các thông tin để các cán bộ có thể dễ dàng thực hiện; Rà soát và cập nhật các SOP định kỳ;
- Cán bộ xét nghiệm phải tuyệt đối tuân thủ các quy trình xét nghiệm.
- Thực hiện xét nghiệm: Đối chiếu mẫu với sơ đồ xét nghiệm; thao tác chính xác nhẹ nhàng, tránh tạo bọt, khí dung và các thao tác thừa; làm đủ chứng theo yêu cầu của nhà sản xuất, nên tiến hành nội kiểm chứng; để hạn chế sai sót khi thực hiện xét nghiệm nên có hai cán bộ cùng làm để kiểm tra chéo.
3. Giai đoạn sau xét nghiệm
a) Đọc kết quả
- Kỹ thuật xét nghiệm nhanh: Đọc vùng kiểm chứng trước, nếu có xuất hiện vạch kiểm chứng mới tiến hành đọc vùng phản ứng.
- Kỹ thuật ngưng kết hạt: Đọc trên nền trắng, đủ ánh sáng; Đọc giếng có hạt không gắn kháng nguyên rồi mới đọc giếng có hạt gắn kháng nguyên.
- Kỹ thuật ELISA: Đọc đúng bước sóng, chương trình.
b) Biện luận kết quả
- Kỹ thuật xét nghiệm nhanh: Chỉ đọc kết quả bệnh phẩm khi có xuất hiện vạch tại vùng kiểm chứng.
- Kỹ thuật ngưng kết hạt:
+ Kiểm tra tính hợp lệ của phản ứng dựa trên các mẫu chứng: Giếng chứng có hạt không gắn kháng nguyên phải lắng ở đáy giếng; mẫu kiểm chứng và chứng dương của sinh phẩm phải đạt tiêu chuẩn của nhà sản xuất.
+ Biện luận kết quả tại giếng có các hạt gắn kháng nguyên: Tùy vào mức độ ngưng kết và biện luận kết quả của mẫu thử theo hướng dẫn của nhà sản xuất; Trong trường hợp cả hai giếng đều xảy ra hiện tượng ngưng kết thì cần thực hiện thao tác hấp phụ.
- Kỹ thuật ELISA/hóa phát quang/điện hóa phát quang trên máy miễn dịch tự động: Kiểm tra tính hợp lệ của phản ứng dựa trên các mẫu chứng. Chỉ biện luận kết quả khi các mẫu chứng đạt tiêu chuẩn của nhà sản xuất. Phòng xét nghiệm phải chạy mẫu chuẩn máy và kết quả phải đạt yêu cầu của nhà sản xuất.
c) Ghi chép và lưu trữ sổ sách xét nghiệm
- Các kết quả xét nghiệm phải được ghi chép đầy đủ chính xác và lưu giữ trong sổ xét nghiệm theo quy định; Khi xảy ra sai sót phải sử dụng bút gạch ngang và ghi kết quả đúng vào dòng phía dưới kèm theo ký xác nhận của cán bộ xét nghiệm hoặc phụ trách phòng xét nghiệm.
- Các kết quả xét nghiệm được ghi chép vào sổ xét nghiệm theo từng mẫu bệnh phẩm.
- Cán bộ phụ trách phòng xét nghiệm chịu trách nhiệm kiểm tra thông tin ghi chép sổ xét nghiệm định kỳ.
d) Quản lý và tiêu hủy mẫu
- Các mẫu dương tính hoặc không xác định: lưu trong các ống nghiệm chịu được nhiệt độ âm sâu; theo sơ đồ lưu mẫu; ở nhiệt độ âm 20oC hoặc lạnh hơn trong thời gian 2 năm kể từ ngày có kết quả xét nghiệm khẳng định.
- Thông tin của các mẫu lưu phải ghi chép đầy đủ và chính xác vào sổ lưu mẫu, có sơ đồ mã hóa mẫu lưu được quy định theo năm và vị trí lưu và tránh nhầm lẫn qua các năm.
- Tiến hành việc hủy các mẫu lưu khi hết thời hạn và phải lưu trữ biên bản hủy mẫu theo quy định.
e) Trả kết quả xét nghiệm
- Phiếu trả kết quả xét nghiệm theo đúng biểu mẫu của Bộ Y tế sử dụng cho phòng xét nghiệm HIV.
- Cán bộ phụ trách phòng xét nghiệm cần kiểm tra các thông tin và kết quả trước khi ký vào kết quả trả cho người được làm xét nghiệm.
III. GIÁM SÁT ĐẢM BẢO CHẤT LƯỢNG XÉT NGHIỆM
1. Đánh giá chất lượng thông qua chương trình nội kiểm tra (chương trình IQC)
Nội kiểm là quá trình đánh giá chất lượng xét nghiệm sử dụng hệ thống kiểm chứng với mục đích kiểm tra tính chính xác, mức độ tin cậy và độ ổn định của kết quả xét nghiệm.
Nội kiểm gồm có 2 hình thức: Sử dụng mẫu chứng của nhà sản xuất; sử dụng mẫu nội kiểm.
a) Mẫu chứng của nhà sản xuất bắt buộc phải thực hiện.
- Với sinh phẩm xét nghiệm nhanh các chứng nội kiểm đã được nhà sản xuất thiết kế nằm ngay trên mỗi thanh hay phiến xét nghiệm. Xét nghiệm chỉ hợp lệ khi dấu hiệu nội kiểm này được hiển thị rõ, khi đó các kết quả xét nghiệm mẫu bệnh phẩm mới có giá trị. Nếu các dấu hiệu nội kiểm này không hiện ra thì kết quả phản ứng được coi là không hợp lệ khi đó không được phép đọc kết quả xét nghiệm mẫu bệnh phẩm.
- Với sinh phẩm ngưng kết hạt, các mẫu nội kiểm là mẫu chứng dương tính được xét nghiệm cùng với mẫu bệnh phẩm mỗi khi làm xét nghiệm. Kết quả xét nghiệm chỉ có giá trị khi mẫu chứng này hợp lệ.
-Với sinh phẩm ELISA/hóa phát quang/điện hóa phát quang các mẫu nội kiểm là các chứng âm, chứng dương hoặc các mẫu chứng ngưỡng. Kết quả xét nghiệm có giá trị khi các mẫu chứng này có giá trị phù hợp theo yêu cầu của từng loại sinh phẩm. Khi các giá trị mẫu chứng không hợp lệ cần phải làm xét nghiệm lại.
b) Mẫu chứng nội kiểm (là chứng được thực hiện thêm ngoài chứng của nhà sản xuất): khuyến cáo sử dụng nếu có điều kiện.
- Tần suất thực hiện:
+ Kỹ thuật ELISA/hóa phát quang/điện hóa phát quang nên thực hiện cùng với mỗi lần làm xét nghiệm.
+ Kỹ thuật xét nghiệm nhanh/đơn giản: Với Cơ số mẫu > 20 mẫu/ngày thực hiện 01 lần/ngày, với cơ số mẫu ≤ 20 mẫu/ngày thì đủ 20 mẫu thực hiện một lần.
- Ghi chép và giám sát kết quả:
+ Kỹ thuật ELISA/hóa phát quang/điện hóa phát quang: Cập nhật các kết quả chạy mẫu nội kiểm vào biểu đồ Levy Jenning; Phân tích kết quả có vi phạm quy tắc Wesgard không, nếu vi phạm cần thực hiện lại xét nghiệm và không được trả kết quả xét nghiệm cho người được làm xét nghiệm.
+ Kỹ thuật xét nghiệm nhanh/đơn giản: Các kết quả được điền vào sổ theo dõi nội kiểm, nếu kết quả không đạt cần thực hiện lại.
2. Đánh giá chất lượng xét nghiệm từ bên ngoài (chương trình ngoại kiểm - EQAS)
Đây là chương trình kiểm soát chất lượng và đánh giá năng lực phòng xét nghiệm một cách có hệ thống thông qua một tổ chức độc lập.
Thông qua chương trình, kết quả xét nghiệm của các đơn vị tham gia được so sánh với nhau hoặc với kết quả của bộ mẫu ngoại kiểm.
Các phòng xét nghiệm HIV phải tham gia chương trình ngoại kiểm theo quy định.
Mục tiêu của chương trình ngoại kiểm là:
+ Đánh giá chất lượng xét nghiệm của các đơn vị tham gia giúp phát hiện các sai sót và đưa ra các hướng khắc phục.
+ Khuyến khích việc thực hành tốt phòng xét nghiệm và sử dụng sinh phẩm có chất lượng.
Chương trình ngoại kiểm phải đảm bảo tính bí mật thông tin các đơn vị tham gia thông qua việc mã hóa.
Chương trình ngoại kiểm bao gồm các bước:
+ Thông báo về chương trình đến các phòng xét nghiệm.
+ Các phòng xét nghiệm đăng ký tham gia.
+ Các bộ mẫu ngoại kiểm được gửi đến các đơn vị đăng ký.
+ Các đơn vị tham gia thực hiện xét nghiệm bộ mẫu ngoại kiểm theo thường quy và gửi kết quả cho đơn vị cung cấp theo hướng dẫn.
+ Đơn vị cung cấp gửi kết quả bộ mẫu ngoại kiểm cho đơn vị tham gia.
+ Đơn vị cung cấp phân tích, tổng hợp và gửi báo cáo kết quả chương trình ngoại kiểm tới đơn vị tham gia.
Thông qua kết quả của chương trình ngoại kiểm, phòng xét nghiệm phải tìm hiểu, phát hiện các sai sót và tiến hành việc khắc phục cải thiện chất lượng xét nghiệm.
Đơn vị cung cấp chương trình ngoại kiểm hỗ trợ kỹ thuật khi cần.
3. Kiểm tra, giám sát.
- Kiểm tra định kỳ:
Viện Vệ sinh dịch tễ Trung ương, Viện Pasteur Thành phố Hồ Chí Minh, Viện Pasteur Nha Trang, Viện Vệ sinh tễ Tây Nguyên kiểm tra giám sát hoạt động xét nghiệm của các phòng xét nghiệm HIV trong khu vực được phân công phụ trách định kỳ 1 lần/năm.
Trung tâm Phòng, chống HIV/AIDS tỉnh tổ chức việc kiểm tra giám sát hoạt động xét nghiệm cho các đơn vị sàng lọc trên địa bàn tỉnh 6 tháng/lần.
- Kiểm tra đột xuất: Viện Vệ sinh dịch tễ Trung ương, Viện Pasteur Thành phố Hồ Chí Minh, Viện Pasteur Nha Trang, Viện Vệ sinh tễ Tây Nguyên chịu trách nhiệm tổ chức các đoàn kiểm tra, giám sát theo yêu cầu của Cục Phòng, chống HIV/AIDS, Bộ Y tế.
- Kiểm tra chéo: Kiểm tra chéo giữa các đơn vị nhằm đánh giá, rút kinh nghiệm để nâng cao chất lượng xét nghiệm.
- Đánh giá nội bộ: Giúp các đơn vị tự nhìn nhận, phát hiện và khắc phục các hạn chế trong công tác xét nghiệm./.
PHỤ LỤC 1
HƯỚNG DẪN LẤY MÁU, VẬN
CHUYỂN, BẢO QUẢN VÀ TIÊU HỦY MẪU XÉT NGHIỆM HIV
(Ban
hành kèm theo Quyết định số 1098/QĐ-BYT ngày 04 tháng 4 năm 2013 của Bộ trưởng
Bộ Y tế)
I. LẤY MẪU MÁU
1. Lấy máu đầu ngón tay
a) Chuẩn bị dụng cụ: Kim/lưỡi chích dùng một lần có lẫy (lancet) chuyên dụng, ống mao quản có thể tích phù hợp, găng tay, bông thấm nước vô trùng, cồn 70º hoặc cồn I ốt, băng cá nhân, thùng đựng chất thải theo quy định.
b) Chuẩn bị lấy máu
- Điền đầy đủ các thông tin về người được làm xét nghiệm (họ tên hoặc mã số và năm sinh/tuổi) và ngày lấy mẫu trên phiếu xét nghiệm và trên thanh sinh phẩm;
- Rửa tay và đeo găng tay.
c) Tiến hành lấy máu
- Yêu cầu người được làm xét nghiệm làm ấm bàn tay bằng cách xoa hai tay với nhau hoặc rửa tay bằng nước ấm;
- Xác định vị trí chích máu: Vị trí chích máu tốt nhất là mặt bên (trái hoặc phải của ngón tay thứ 3 (ngón giữa) hoặc thứ 4 (ngón áp út));
- Yêu cầu người được làm xét nghiệm duỗi bàn tay xuống phía dưới;
- Sát khuẩn vị trí lấy máu bằng cồn 70o và để khô trong vòng 30 giây;
- Ấn lẫy kim/lưỡi chích một cách vuông góc với mặt da đầu ngón tay một cách nhanh, mạnh dứt khóat. Đảm bảo giữ kim chích đúng góc và không làm nghiêng;
- Lau bỏ giọt máu đầu tiên (vì giọt máu đầu tiên thường chứa dịch tổ chức, tế bào kẽ không đủ lượng máu cho xét nghiệm);
- Đợi cho đến khi máu chảy thành giọt lớn, dùng ống mao quản hút đủ thể tích yêu cầu (không bóp nặn vùng chích máu để tiết ra dịch tổ chức mô xung quanh sẽ ảnh hưởng đến chất lượng mẫu);
- Bỏ kim/lưỡi chích vào hộp đựng các vật sắc nhọn và ống mao quản dùng đã hút mẫu máu vào hộp đựng rác thải y tế;
- Sát trùng lại vị trí đã lấy máu bằng cồn 70o và băng lại;
- Mẫu sau khi lấy cần tiến hành xét nghiệm theo hướng dẫn của nhà sản xuất.
Lưu ý:
Trường hợp xét nghiệm cho kết quả phản ứng (+) thì cần lấy máu tĩnh mạch của người được làm xét nghiệm để thực hiện xét nghiệm theo quy định.
2. Lấy máu tĩnh mạch
a) Chuẩn bị dụng cụ: bơm kim tiêm vô trùng hoặc bộ dụng cụ lấy máu bằng ống hút chân không (vacutainer, kim, giá đỡ), ống nghiệm nhựa có nắp đậy, ống nghiệm có chất chống đông (khi cần thu thập mẫu huyết tương), găng tay, khẩu trang, dây ga rô, bông thấm nước vô trùng, cồn 70º, bút dạ (loại mực chịu nước), giá để ống nghiệm, thùng đựng các vật sắc nhọn và rác thải y tế .
b) Chuẩn bị lấy máu
- Điền đầy đủ các thông tin về người được làm xét nghiệm (họ tên/mã số và năm sinh/tuổi) và ngày lấy mẫu trên phiếu xét nghiệm và ống đựng mẫu.
- Rửa tay và đeo găng tay.
c) Tiến hành lấy máu
- Xác định vị trí lấy máu (tĩnh mạch) và sát khuẩn bằng cồn 70o và để khô trong vòng 30 giây.
- Đưa kim vào tĩnh mạch lấy 3- 4 ml máu cho vào ống đựng máu. Có thể dùng bơm kim tiêm loại 5ml (đầu kim cỡ 21G - 23G) để lấy máu hoặc dùng bộ dụng cụ lấy máu với ống hút chân không (vacutainer). Nếu dùng bơm kim tiêm để lấy máu thì tháo đầu kim ra, để bơm tiêm chếch với thành ống nghiệm và bơm từ từ cho máu chảy theo thành ống nghiệm tránh làm vỡ hồng cầu.
- Thải bỏ đầu kim vào hộp đựng các vật sắc nhọn và bơm tiêm hoặc giá đỡ ống lấy máu bẩn vào hộp đựng rác thải y tế;
- Sát trùng lại vị trí lấy máu bằng cồn 70o và băng lại.
- Tách huyết thanh/huyết tương:
+ Sau khi lấy máu phải để ổn định 30 phút và không quá 2 giờ ở nhiệt độ phòng, tiến hành tách huyết thanh/huyết tương. Trường hợp không tách được huyết thanh/huyết tương trong vòng 2 giờ, để mẫu ổn định ở nhiệt độ phòng 30 phút sau đó bảo quản ở nhiệt độ 4-8oC và cần phải tách huyết thanh/huyết tương trong vòng 24 giờ.
+ Sử dụng máy ly tâm phải thăng bằng các ống nghiệm trước khi ly tâm. Tiến hành ly tâm tốc độ 2000 - 2500 vòng/phút trong vòng 10 phút. Tách phần huyết thanh/huyết tương vào một ống nghiệm nhựa rồi đóng chặt nắp.
+ Không có máy ly tâm: Để ống nghiệm trên giá trong vòng 30 phút sau đó để vào tủ lạnh ở nhiệt độ 4-8oC, tối thiểu 2 giờ nhưng không quá 24 giờ phải tách huyết thanh/huyết tương cho vào một ống nghiệm nhựa rồi đóng chặt nắp.
Thể tích huyết thanh/huyết tương tối thiểu thu thập được là 1,5ml.
II. QUY TRÌNH VẬN CHUYỂN MẪU
1. Đóng gói mẫu
- Đeo găng tay đóng chặt các nắp của ống mẫu và xếp tất cả các ống mẫu theo phương thẳng đứng vào trong giá đựng mẫu. Dùng băng dính cố định các ống mẫu trong giá đựng bệnh phẩm và để trong túi nylon dán kín.
- Đặt túi nylon có chứa mẫu và cho đủ vật liệu thấm hút (bông hoặc giấy thấm nước) vào thùng vận chuyển mẫu.
- Đặt các túi tích lạnh vào thùng đựng mẫu để đảm bảo mẫu được bảo quản từ 2-8oC trong quá trình vận chuyển.
- Đóng nắp thùng đựng mẫu và chốt khóa lại. Trường hợp không có chốt khóa thì dùng băng dính dán xung quanh.
- Dán hoặc in ký hiệu nguy hiểm sinh học và số điện thoại liên hệ trong trường hợp khẩn cấp bên ngoài của hộp đựng mẫu bệnh phẩm. Trường hợp không có nhãn nguy hiểm sinh học thì phải có ghi rõ mọi thông tin và số điện thoại liên hệ bên ngoài của hộp vận chuyển mẫu bệnh phẩm.
Lưu ý: Không để danh sách mẫu vào trong hộp vận chuyển mẫu.
2. Vận chuyển mẫu
- Vận chuyển mẫu bệnh phẩm phải tuân thủ các quy định của quốc gia và chính quyền địa phương về vận chuyển các tác nhân có khả năng gây bệnh.
- Nơi gửi mẫu nên gọi điện báo trước cho phòng xét nghiệm biết thời gian bệnh phẩm sẽ tới để phòng xét nghiệm bố trí cán bộ tiếp nhận.
- Bệnh phẩm gửi đi phải kèm theo phiếu xét nghiệm điền đầy đủ các thông tin.
- Mẫu bệnh phẩm phải được bảo quản lạnh trong suốt quá trình vận chuyển.
- Trong quá trình vận chuyển mẫu phải buộc chặt hộp chứa mẫu bệnh phẩm vào giá chở hàng, đảm bảo gọn gàng, tránh đổ, vỡ.
3. Tiếp nhận mẫu
- Kiểm tra nhiệt độ trong hộp vận chuyển, kiểm tra tình trạng mẫu, đối chiếu thông tin trên ống đựng máu, phiếu xét nghiệm và sổ vận chuyển mẫu.
- Thông báo cho nơi gửi xét nghiệm lấy lại mẫu trong các trường hợp: máu bị đông, huyết thanh đã bị tán huyết, mẫu không được vận chuyển đúng nhiệt độ, mẫu không đủ thể tích yêu cầu, mẫu được chuyển đến quá thời gian quy định.
- Thông báo cho nơi gửi mẫu xét nghiệm bổ sung thông tin trong trường hợp: thiếu thông tin về địa chỉ, ngày, thu thập mẫu trên phiếu xét nghiệm.
- Ký nhận vào phiếu gửi mẫu và ghi chép thông tin vào sổ nhận mẫu.
III. BẢO QUẢN MẪU
- Mẫu huyết thanh/huyết tương nếu xét nghiệm trong vòng 7 ngày phải bảo quản ở nhiệt độ 4-8oC. Nếu tiến hành xét nghiệm sau 7 ngày cần bảo quản ở nhiệt độ âm 20oC hoặc lạnh hơn. Tuy nhiên mẫu không được tan đông quá 3 lần.
- Lưu mẫu huyết thanh dương tính hoặc nghi ngờ trong ở nhiệt độ âm 20oC hoặc lạnh hơn trong thời gian ít nhất 2 năm.
- Các ống nghiệm lưu mẫu ở nhiệt độ âm sâu phải là các ống nghiệm chuyên dụng có nắp xoáy chặt. Các ống nghiệm xếp trong hộp chuyên dụng. Phải ghi rõ thông tin về mẫu trên ống nghiệm bằng loại mực không xóa được.
- Các mẫu khi lưu phải có mã số và ghi chép trong sổ lưu mẫu theo quy định.
IV. TIÊU HỦY MẪU XÉT NGHIỆM.
1. Tiêu hủy mẫu xét nghiệm: Tuân thủ theo quy định tại Quyết định số 43/2007/QĐ-BYT ngày 30/11/2007 của Bộ Y tế về việc ban hành Qui chế quản lý chất thải y tế và các quy định pháp luật có liên quan.
2. Hủy mẫu lưu dương tính và nghi ngờ: sau khi hết thời gian lưu mẫu theo quy định, việc hủy mẫu cần phải lập biên bản ghi rõ thời gian và danh sách các mẫu đã hủy. Biên bản này phải lưu trong thời gian 5 năm kể từ ngày hủy mẫu./.
PHỤ LỤC 2
PHƯƠNG PHÁP VÀ KỸ THUẬT
XÉT NGHIỆM
(Ban
hành kèm theo Quyết định số 1098/QĐ-BYT ngày 04 tháng 4 năm 2013 của Bộ tr ưởn
g Bộ Y tế)
I. PHƯƠNG PHÁP XÉT NGHIỆM GIÁN TIẾP
1. Thông tin chung
Tìm kháng thể kháng HIV là phương pháp thông thường được sử dụng trong xét nghiệm an toàn truyền máu, giám sát dịch tễ và chẩn đoán nhiễm HIV ở người lớn và trẻ em trên 18 tháng tuổi.
Kháng thể kháng HIV có thể được phát hiện trong máu người từ 4 đến 6 tuần sau khi nhiễm vi rút và tồn tại lâu dài trong máu người nhiễm.Trong một số trường hợp kháng thể kháng HIV có thể xuất hiện muộn hơn.
Giai đoạn cửa sổ là giai đoạn cơ thể người mang vi rút HIV nhưng chưa sinh ra kháng thể để có thể phát hiện được bằng các xét nghiệm thông thường nhưng vẫn có khả năng lây nhiễm HIV cho người khác.
Các xét nghiệm cần phát hiện được kháng thể kháng HIV-1 và HIV-2 trong đó có khả năng phát hiện được tất cả các phân nhóm của HIV-1 trong đó chú ý đến phân nhóm M, N, O.
2. Các kỹ thuật xét nghiệm nhanh hoặc đơn giản
Các xét nghiệm nhanh hoặc đơn giản gồm: ngưng kết hạt vi lượng; miễn dịch chấm - thấm; miễn dịch lọc; miễn dịch sắc ký.
Đặc điểm chung của các xét nghiệm nhanh là tương đối đơn giản, dễ thực hiện, không đòi hỏi máy móc chuyên biệt. Một số loại xét nghiệm nhanh có thể dùng huyết thanh, huyết tương hoặc máu toàn phần. Các xét nghiệm nhanh cho kết quả trong một thời gian tương đối ngắn và đọc được bằng mắt thường.
Các sinh phẩm chẩn đoán nhanh thường được dùng ở những phòng thí nghiệm có số lượng mẫu < 40="" mẫu/ngày,="" trong="" các="" trường="" hợp="" cần="" chẩn="" đoán="" khẩn="" cấp="" cần="" có="" kết="" quả="">
2.1. Các xét nghiệm ngưng kết hạt vi lượng.
Những hạt hữu hình (gelatin, latex, hồng cầu) được gắn với các thành phần kháng nguyên của vi rút HIV-1/HIV-2 sẽ cho phản ứng ngưng kết khi có sự hiện diện của kháng thể đặc hiệu với HIV nếu có trong mẫu thử.
2.2. Các xét nghiệm miễn dịch chấm - thấm.
- Là kỹ thuật dựa trên nguyên tắc miễn dịch đánh dấu trên màng lọc.
- Màng phản ứng chứa những hạt vi lượng bao phủ kháng nguyên HIV-1 và HIV-2, đồng thời có một vùng chứng để kiểm tra phản ứng.
- Kháng thể kháng HIV có trong huyết thanh hoặc huyết tương người được làm xét nghiệm sẽ gắn với kháng nguyên trên màng lọc. Sau đó, phức hợp kháng nguyên-kháng thể này được phát hiện bởi cộng hợp có gắn men cho phản ứng hiện màu với cơ chất.
2.3. Các xét nghiệm miễn dịch sắc ký.
- Mẫu xét nghiệm sẽ được nhỏ lên vùng nhỏ mẫu thử. Huyết thanh/huyết tương sẽ thấm qua vùng có chứa cộng hợp là kháng nguyên vi rút đã gắn với một chất đánh dấu mầu và tiếp tục dịch chuyển qua vùng phản ứng đã cố định kháng nguyên. Nếu mẫu thử có kháng thể đặc hiệu với HIV sẽ cho phản ứng dương tính là một vạch màu ở vị trí này. Cộng hợp kháng nguyên vi rút gắn đánh dấu mầu tiếp tục dịch chuyển lên vùng chứng phía trên là vị trí đã cố định sẵn kháng thể đơn dòng đặc hiệu với HIV và cho một vạch phản ứng màu (vạch chứng của phản ứng).
- Xét nghiệm dương tính khi có hai vạch màu ở vùng phản ứng và vùng kiểm chứng.
- Xét nghiệm âm tính khi chỉ có vạch màu ở vùng kiểm chứng.
- Xét nghiệm không có giá trị nếu không có vạch màu ở vùng chứng, khi đó phải thực hiện lại xét nghiệm mẫu đó trên thanh sinh phẩm mới.
2.4. Ưu điểm và nhược điểm của các kỹ thuật xét nghiệm nhanh
- Ưu điểm:
+ Thuận lợi khi số lượng mẫu ít.
+ Dễ thực hiện, cho kết quả nhanh, có thể đọc kết quả bằng mắt thường.
+ Không đòi hỏi các trang thiết bị.
+ Dễ bảo quản sinh phẩm.
+ Cán bộ xét nghiệm có thể được đào tạo nhanh.
- Nhược điểm:
+ Không thuận lợi khi số mẫu xét nghiệm nhiều.
+ Không lưu được dữ liệu kết quả.
+ Kết quả đọc phụ thuộc chủ quan vào người đọc.
3. Các kỹ thuật miễn dịch đánh dấu (ELISA/hóa phát quang/điện hóa phát quang)
3.1. Dựa trên nguyên tắc xét nghiệm, các kỹ thuật miễn dịch đánh dấu chia thành các nhóm sau:
- Kỹ thuật Sandwich
+ Kháng thể kháng HIV có trong mẫu thử sẽ kết hợp đặc hiệu với kháng nguyên vi rút đã được cố định trên giá đỡ. Phức hợp kháng nguyên - kháng thể sẽ được phát hiện bởi cộng hợp là các kháng nguyên vi rút gắn các chất đánh dấu (men, hóa phát quang) khi cho phản ứng hiện màu với cơ chất.
+ Giá trị mật độ quang (OD: optical density) của phản ứng màu tỷ lệ thuận với lượng kháng thể kháng HIV hiện diện trong mẫu thử.
- Kỹ thuật gián tiếp
+ Kháng thể kháng HIV có trong mẫu thử sẽ kết hợp đặc hiệu với kháng nguyên vi rút HIV đã được cố định sẵn trên giá đỡ. Phức hợp kháng nguyên - kháng thể này được phát hiện bởi một cộng hợp là một kháng thể kháng immunoglobuline người (Ig) có gắn chất đánh dấu và sẽ cho phản ứng hiện màu/phát quang với một cơ chất thích hợp. Giá trị mật độ quang của phản ứng màu/phát quang tỷ lệ thuận với lượng kháng thể kháng HIV hiện diện trong mẫu thử.
- Kỹ thuật cạnh tranh
+ Kháng thể kháng HIV có trong mẫu thử sẽ cạnh tranh với cộng hợp là kháng thể kháng HIV có gắn với chất đánh dấu để kết hợp với các kháng nguyên của vi rút đã cố định trên giá đỡ.
+ Giá trị mật độ quang tỷ lệ nghịch với lượng kháng thể trong mẫu thử.
- Kỹ thuật phát hiện đồng thời kháng nguyên và kháng thể
+ Một số sinh phẩm dùng kỹ thuật phát hiện đồng thời kháng nguyên vi rút (p24) và kháng thể kháng HIV cho phép phát hiện sớm nhiễm HIV trong giai đoạn chuyển đổi huyết thanh. Kháng nguyên p24 hoặc các kháng thể kháng HIV hiện diện trong mẫu thử kết hợp đặc hiệu với kháng thể kháng p24 và các kháng nguyên vi rút được gắn trên giá đỡ. Phức hợp kháng nguyên - kháng thể sẽ được phát hiện bởi các cộng hợp gắn chất đánh dấu cho phản ứng hiện màu/phát quang sau khi cho cơ chất.
+ Các sinh phẩm phát hiện đồng thời kháng nguyên p24 và kháng thể kháng HIV thường được dùng trong xét nghiệm an toàn truyền máu.
3.2. Dựa trên nguyên lý chuẩn bị các kháng nguyên, các sinh phẩm được chia thành 4 thế hệ:
- Sinh phẩm thế hệ thứ nhất sử dụng kháng nguyên là vi rút toàn phần được ly giải và tinh chế từ các tế bào đã gây nhiễm với HIV. Các sinh phẩm này có độ nhạy và độ đặc hiệu hạn chế.
- Sinh phẩm thế hệ thứ hai dùng các kháng nguyên là protein tái tổ hợp. Sinh phẩm có độ nhạy và độ đặc hiệu cao hơn.
- Sinh phẩm thế hệ ba sử dụng các kháng nguyên là các peptite tổng hợp và các protein tái tổ hợp. Độ nhạy và độ đặc hiệu được cải thiện rõ rệt.
- Sinh phẩm thế hệ thứ tư phát hiện đồng thời kháng nguyên P24 và kháng thể có trong mẫu thử. Sinh phẩm này cho phép phát hiện nhiễm HIV trong giai đoạn chuyển đổi huyết thanh và là sinh phẩm được khuyến cáo nên lựa chọn cho kiểm tra an toàn trong truyền máu.
Các sinh phẩm chẩn đoán ngày càng được hoàn thiện để có thể phát hiện sớm và chính xác nhiễm HIV, rút ngắn thời gian cửa sổ huyết thanh.
3.3. Ưu điểm và hạn chế của các kỹ thuật miễn dịch đánh dấu:
- Ưu điểm
+ Cho phép thực hiện đồng thời nhiều mẫu. Có thể dùng máy tự động giảm bớt thao tác cho người làm xét nghiệm, tránh sai sót và lây nhiễm.
+ Đọc kết quả bằng máy không phụ thuộc vào chủ quan của người làm xét nghiệm.
+ Các máy hóa phát quang, điện hóa phát quang cho kết quả nhanh trong vòng từ 10-20 phút và có công suất lớn.
+ Có thể lưu các bảng kết quả và các thông số kỹ thuật thuận lợi cho việc kiểm tra đánh giá chất lượng xét nghiệm.
- Hạn chế
+ Cần có sự đầu tư cho trang thiết bị ban đầu và bảo dưỡng, hiệu chuẩn, hiệu chỉnh máy móc. Đối với các máy miễn dịch tự động (hóa phát quang, điện hóa phát quang, miễn dịch men vi hạt) chỉ sử dụng được với sinh phẩm sử dụng đồng bộ với máy.
+ Các sinh phẩm phải bảo quản ở nhiệt độ lạnh (4-8oC).
+ Thời gian thực hiện xét nghiệm ELISA từ 2-3 giờ.
+ Chỉ thích hợp với những nơi có số lượng mẫu > 40 mẫu/ngày.
4. Kỹ thuật WESTERN-BLOT
Kỹ thuật Western-blot được chỉ định để khẳng định các mẫu đã có kết quả dương tính với 2 xét nghiệm khác.
Đây là một kỹ thuật giá thành cao nên hiện nay Tổ chức Y tế thế giới không khuyến cáo thực hiện thường quy ở những nước đang phát triển.
Để xác định một trường hợp nhiễm HIV có thể dùng phối hợp ba xét nghiệm khác nhau về nguyên lý hoặc cách chuẩn bị kháng nguyên.
Kỹ thuật Western-blot được cân nhắc thực hiện trong trường hợp các kết quả xét nghiệm không xác định hoặc khó biện luận.
- Nguyên tắc: là một kỹ thuật theo nguyên lý ELISA gián tiếp thực hiện trên băng giấy đã cố định các thành phần kháng nguyên của vi rút ở những vị trí tương ứng theo trọng lượng phân tử. Kỹ thuật Western-blot cho phép xác định kháng thể kháng từng thành phần khác nhau của protein vi rút. Có Western-blot riêng cho HIV-1 và HIV-2.
- Kỹ thuật: Ủ huyết thanh của mẫu thử với băng giấy. Nếu trong mẫu thử có các kháng thể kháng HIV thì chúng sẽ gắn đặc hiệu lên các protein là kháng nguyên tương ứng và được phát hiện bằng cộng hợp là kháng thể kháng Immunoglobuline người đánh dấu bằng enzyme cho phản ứng màu với cơ chất.
- Kết quả: Vị trí các băng màu tương ứng với kháng thể đặc hiệu với thành phần protein vi rút tương ứng
II. PHƯƠNG PHÁP XÉT NGHIỆM TRỰC TIẾP
1. Khái niệm: Phương pháp xét nghiệm trực tiếp tìm HIV (hay còn gọi chung là xét nghiệm vi rút học) như phát hiện kháng nguyên vi rút, các axit nucleic hoặc phân lập vi rút.
Phương pháp xét nghiệm trực tiếp được dùng để phát hiện nhiễm HIV ở trẻ dưới 18 tháng tuổi, chẩn đoán sớm nhiễm HIV ở người lớn trong giai đoạn cửa sổ hoặc khi xét nghiệm bằng phương pháp gián tiếp tìm kháng thể cho kết quả không rõ ràng.
2. Phát hiện kháng nguyên p24 (antigen p24)
Kháng nguyên p24 là protein cấu thành của lõi vi rút, bao bọc các chất liệu di truyền và là một chỉ số phản ánh sự nhân lên của vi rút. Kháng nguyên p24 tồn tại dưới dạng tự do hoặc trong phức hợp kháng nguyên-kháng thể.
Phát hiện kháng nguyên p24 thông thường được sử dụng trong:
- Chẩn đoán nhiễm HIV ở trẻ sơ sinh: Đây là một kỹ thuật kém nhạy nhưng rất đặc hiệu. Hiện nay các sinh phẩm phát hiện kháng nguyên p24 đã được hoàn thiện để nâng cao độ nhạy.
- Phát hiện sớm giai đoạn mới nhiễm HIV: Trong giai đoạn đầu mới nhiễm HIV, kháng nguyên p24 có thể được phát hiện trước khi có sự biến đổi huyết thanh, ở giai đoạn cửa sổ khi chưa có kháng thể.
- Theo dõi diễn tiến nhiễm HIV: Kháng nguyên p24 có thể được phát hiện rất sớm ở giai đoạn mới nhiễm. Cùng với sự xuất hiện kháng thể, nồng độ kháng nguyên p24 tự do trong máu giảm. Ở giai đoạn cuối, cùng với sự giảm kháng thể kháng p24, sự tái xuất hiện và gia tăng nồng độ p24 tự do là một tiên lượng chuyển sang AIDS.
- Theo dõi đáp ứng điều trị với thuốc kháng vi rút.
- Phát hiện có sự nhân lên của vi rút trong nuôi cấy tế bào
3. Các kỹ thuật sinh học phân tử phát hiện HIV-ARN hoặc HIV-AND provirus.
- Các kỹ thuật sinh học phân tử được áp dụng trong xét nghiệm phát hiện sớm nhiễm HIV; đo tải lượng vi rút trong theo dõi điều trị.
- Các kỹ thuật PCR và Real Time PCR phát hiện ADN tiền vi rút trong tế bào nhiễm hoặc HIV - ARN trong huyết tương.
- Các nguyên tắc chung của các kỹ thuật sinh học phân tử:
- Nguyên tắc của kỹ thuật PCR: Phản ứng PCR (Polymerase Chain Reaction: phản ứng tổng hợp chuỗi) là kỹ thuật cho phép khuếch đại một lượng rất nhỏ phân tử ADN đích được tách chiết từ các tế bào nhiễm hoặc được tổng hợp từ các ARN của vi rút nhờ enzyme sao chép ngược RT (ADNc).
+ Nguyên tắc của kỹ thuật Real time PCR phát hiện nhiễm HIV (Kỹ thuật PCR theo thời gian thực): Real time PCR là phương pháp cho phép khuếch đại và xác định số lượng các chuỗi ADN được tạo ra trong từng chu kỳ nhiệt.
+ Nguyên tắc của kỹ thuật PCR - lai phân tử: Sản phẩm PCR đã được đánh dấu với biotinyle sẽ được lai ghép với các mẫu dò đặc hiệu với ADN đích đã được cố định trên các giếng của phiến bảng và được phát hiện bởi các tín hiệu cho phép đọc được với máy quang kế (colorimetric)./.
PHỤ LỤC 3
SƠ ĐỒ CHIẾN LƯỢC XÉT NGHIỆM
HIV
(Ban
hành kèm theo Quyết định số 1098/QĐ-BYT ngày 04 tháng 4 năm 2013 của Bộ trưởng
Bộ Y tế)
- (1) Kết quả phản ứng này không được dùng cho mục đích chẩn đoán nhiễm HIV, vì vậy không thông báo kết quả cho người được xét nghiệm.
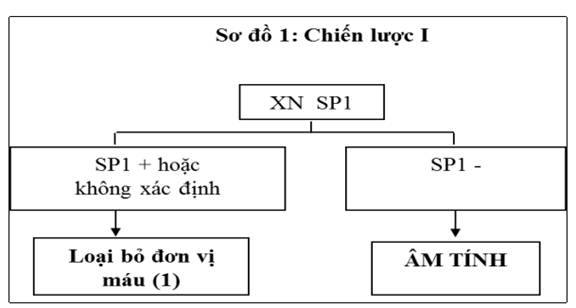
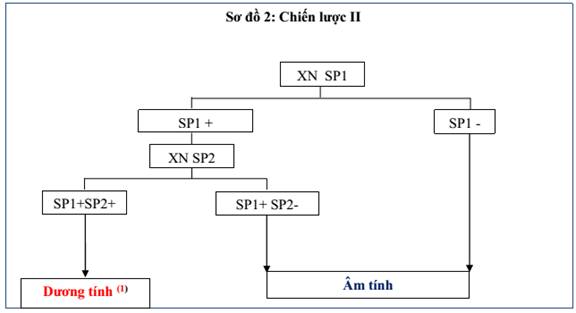
- Các sinh phẩm xét nghiệm SP1, SP2 khác nhau về nguyên lý hoặc cách chuẩn bị kháng nguyên.
- (1) Kết quả này chỉ phục vụ cho mục đích giám sát dịch tễ học HIV/AIDS nên không thông báo cho người được xét nghiệm.
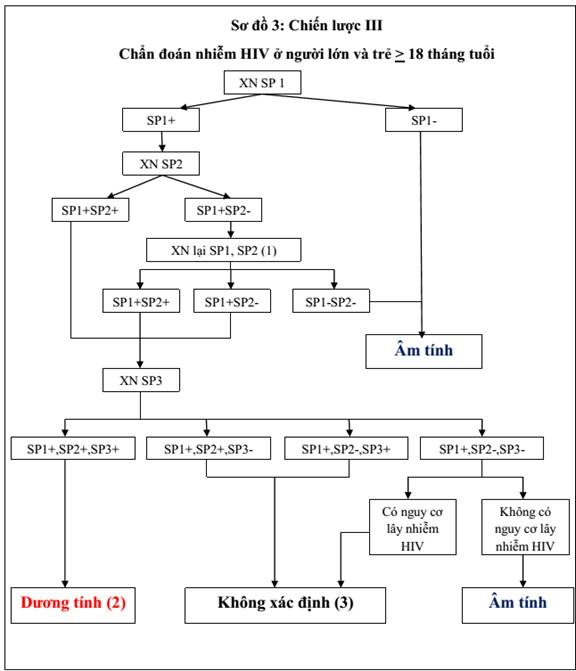
Các sinh phẩm xét nghiệm SP1, SP2, SP3 khác nhau về nguyên lý hoặc cách chuẩn bị kháng nguyên.
(1) Việc xét nghiệm lại bằng SP1, SP2 để kiểm tra loại trừ sai sót khi xét nghiệm bằng sinh phẩm SP1 hoặc SP2.
(2) Kết quả dương tính được dùng để kết luận các trường hợp nhiễm HIV với điều kiện thực hiện xét nghiệm tại phòng xét nghiệm được Bộ Y tế cho phép khẳng định các trường hợp nhiễm HIV.
(3) Trường hợp kết quả xét nghiệm không xác định, đề nghị lấy máu xét nghiệm lại lần thứ 2 sau 14 ngày và biện luận kết quả theo các tình huống sau:
+ Nếu kết quả xét nghiệm lần 2 âm tính thì kết luận là âm tính.
+ Nếu kết quả xét nghiệm lần 2 dương tính theo chiến lược 3 thì kết luận là dương tính.
+ Nếu kết quả lần 2 vẫn không xác định nhưng mức độ phản ứng với sinh phẩm của lần xét nghiệm thứ 2 không có sự thay đổi so với mức độ phản ứng với các sinh phẩm đã sử dụng trong xét nghiệm lần 1 và người được xét nghiệm không thuộc đối tượng có hành vi nguy cơ cao thì kết luận là âm tính.
+ Đề nghị xét nghiệm lần thứ 3 sau 14 ngày nếu kết quả xét nghiệm lần 2 vẫn không xác định trong các tình huống sau:
- Mức độ phản ứng với sinh phẩm của lần xét nghiệm thứ 2 có sự thay đổi tăng so với mức độ phản ứng với các sinh phẩm đã sử dụng trong xét nghiệm lần 1.
- Hoặc nghi ngờ chuyển đổi huyết thanh.
- Hoặc trường hợp mức độ phản ứng với sinh phẩm của lần xét nghiệm thứ 2 không có sự thay đổi so với mức độ phản ứng với các sinh phẩm đã sử dụng trong xét nghiệm lần 1 nhưng người được xét nghiệm thuộc đối tượng có hành vi nguy cơ cao./.


