Nội dung toàn văn Quyết định 4825/QĐ-BYT 2018 tài liệu chuyên môn Hướng dẫn chẩn đoán và điều trị ung thư phổi
|
BỘ
Y TẾ |
CỘNG
HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
|
Số: 4825/QĐ-BYT |
Hà Nội, ngày 06 tháng 08 năm 2018 |
QUYẾT ĐỊNH
VỀ VIỆC BAN HÀNH TÀI LIỆU CHUYÊN MÔN “HƯỚNG DẪN CHẨN ĐOÁN VÀ ĐIỀU TRỊ UNG THƯ PHỔI KHÔNG TẾ BÀO NHỎ”
BỘ TRƯỞNG BỘ Y TẾ
Căn cứ Luật Khám bệnh, chữa bệnh năm 2009;
Căn cứ Nghị định số 75/2017/NĐ-CP ngày 20 tháng 6 năm 2017 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Theo đề nghị của Cục trưởng Cục Quản lý khám, chữa bệnh,
QUYẾT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này tài liệu chuyên môn “Hướng dẫn chẩn đoán và điều trị ung thư phổi không tế bào nhỏ”.
Điều 2. Tài liệu chuyên môn “Hướng dẫn chẩn đoán và điều trị ung thư phổi không tế bào nhỏ” được áp dụng tại các cơ sở khám bệnh, chữa bệnh trong cả nước.
Điều 3. Quyết định này có hiệu lực kể từ ngày ký, ban hành.
Điều 4. Các ông, bà: Chánh Văn phòng Bộ, Chánh thanh tra Bộ, Tổng Cục trưởng, Cục trưởng và Vụ trưởng các Tổng cục, Cục, Vụ thuộc Bộ Y tế, Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc trung ương, Giám đốc các Bệnh viện, Viện trực thuộc Bộ Y tế, Thủ trưởng Y tế các ngành chịu trách nhiệm thi hành Quyết định này./.
|
|
KT.
BỘ TRƯỞNG |
HƯỚNG DẪN
CHẨN ĐOÁN VÀ ĐIỀU TRỊ UNG THƯ PHỔI KHÔNG TẾ BÀO NHỎ (UTPKTBN)
(Ban hành kèm theo Quyết định số
4825/QĐ-BYT ngày 06 tháng
08 năm 2018 của Bộ trưởng Bộ Y
tế)
1. ĐẠI CƯƠNG
Ung thư phổi là một trong 3 ung thư thường gặp nhất và là nguyên nhân gây tử vong hàng đầu do ung thư ở phạm vi toàn cầu. Theo GLOBOCAN 2012, tại Việt Nam, ung thư phổi đứng hàng thứ nhì chỉ sau ung thư gan với tỷ lệ mắc chuẩn theo tuổi ở cả hai giới là 25,2. Bệnh thường gặp ở nam giới, với tỷ lệ mắc chuẩn theo tuổi là 41,1 ở nam và 12,2 ở nữ giới, ước tính mỗi năm có khoảng 22.000 trường hợp mới mắc (16.000 nam và 6.000 nữ) và tử vong khoảng gần 19.600 bệnh nhân.
Ung thư phổi được chia thành hai loại chính là ung thư phổi tế bào nhỏ (small cell lung cancer) - chiếm khoảng 10 - 15% và ung thư phổi không tế bào nhỏ (non small cell lung cancer): chiếm khoảng 85%.
Ung thư phổi không tế bào nhỏ được gây ra bởi nhiều nguyên nhân và yếu tố nguy cơ dưới đây:
• Thuốc lá: ước tính 80 - 90% ung thư phổi liên quan đến thuốc lá. Nguy cơ ung thư phổi tăng theo thời gian và số lượng thuốc lá. Một người hút một gói thuốc mỗi ngày có nguy cơ mắc ung thư phổi gấp 20 lần người không hút thuốc. Nguy cơ ung thư phổi do hút thuốc thụ động cũng được ghi nhận: người sống cùng nhà với người hút thuốc tăng 30% nguy cơ ung thư phổi so với người không cùng hoàn cảnh.
• Tiếp xúc amian: người hút thuốc có tiếp xúc amian có nguy cơ cao gấp 90 lần người không tiếp xúc.
• Bụi phóng xạ và radon: làm tăng nguy cơ ung thư phổi, người tiếp xúc với mức độ radon cao tại nhà ở để mắc ung thư phổi
• Nhiễm khuẩn: Siêu vi bướu nhú ở người (Human papilloma virus (HPV) được quy cho là một nguyên nhân gây ung thư phổi. Gần 25% ung thư phổi trên người không hút thuốc có thể liên quan đến HPV. Chứng đa bướu nhú tái diễn (Recurrent respiratory papillomatosis (RRP)) có thể gây ho, tắc nghẽn hô hấp mạn tính và thoái hóa ác tính. Nhiễm HPV 16/18 thường đi kèm đột biến p53.
• Di truyền: một vài đột biến di truyền là yếu tố liên quan. Đột biến T790M xảy ra trên tế bào mầm kèm theo ung thư biểu mô tuyến của phổi.
• Ô nhiễm không khí: khói bụi trong không khí ô nhiễm có thể làm tăng nguy cơ mắc ung thư phổi, đặc biệt là ung thư biểu mô tuyến.
Tỷ lệ tử vong do ung thư phổi cao do bệnh thường được chẩn đoán vào giai đoạn tiến xa nên cần tăng cường hiệu quả hoạt động tầm soát, phát hiện sớm ung thư phổi. Gần đây chụp cắt lớp điện toán xoắn ốc năng lượng thấp được chấp thuận như biện pháp tầm soát cho đối tượng nguy cơ cao (hút thuốc lá nhiều năm trên 30 gói-năm).
2. CHẨN ĐOÁN
2.1. Lâm sàng
Biểu hiện lâm sàng tùy thuộc vào vị trí và mức độ lan rộng của tổn thương. Trong giai đoạn đầu tổn thương còn khu trú, bệnh nhân thường không có triệu chứng lâm sàng đặc hiệu và được chẩn đoán qua tầm soát hoặc phát hiện tình cờ qua chẩn đoán hình ảnh. Các triệu chứng và dấu hiệu lâm sàng thường được phân thành ba nhóm: triệu chứng tại chỗ tại vùng, triệu chứng do di căn xa và các hội chứng cận ung thư.
a) Các triệu chứng do xâm lấn tại chỗ, tại vùng: liên quan đến tắc nghẽn đường hô hấp, thâm nhiễm nhu mô phổi, và xâm lấn các cấu trúc chung quanh như thành ngực, mạch máu lớn và các tạng trung thất. Các triệu chứng thường gặp bao gồm:
• Ho: gặp trong khoảng 80% bệnh nhân, thường thấy thay đổi về tần suất và mức độ trên người hút thuốc, có thể ho khan hoặc kèm theo khạc đờm.
• Ho ra máu
• Khó thở
• Viêm phổi tái diễn một vị trí
• Tràn dịch màng phổi
• Đau ngực
• Đau vai, tay (hội chứng Pancoast Tobias)
• Hội chứng Homer (sụp mí, co đồng tử, không ra mồ hôi nửa mặt)
• Triệu chứng do chèn ép: khó nuốt, khàn tiếng, hội chứng tĩnh mạch chủ trên...
b) Các triệu chứng do di căn não, xương, chèn ép tủy sống...
• Di căn não: nhức đầu, buồn nôn, nôn, rối loạn nhận thức, vận động, triệu chứng thần kinh khu trú...
• Di căn xương: đau, giới hạn vận động, cảm giác...
• Chèn ép tủy sống: tê, yếu, mất vận động chi, rối loạn cơ tròn...
c) Các hội chứng cận ung thư:
• Không đặc hiệu: sụt cân (có hoặc không kèm chán ăn)
• Hội chứng tăng tiết kháng lợi niệu (SIADH: syndrome of inappropriate antidiuretic hormone secretion)
• Hội chứng tăng tiết ACTH
• Hội chứng Lambert-Eaton
• Hội chứng phì đại xương khớp do phổi
• Hội chứng carcinoid
• Các hội chứng huyết học hiếm gặp khác như thiếu máu, tăng bạch cầu ...
2.2. Cận lâm sàng: giúp chẩn đoán xác định và phân biệt.
a) Chẩn đoán hình ảnh
• X quang ngực thẳng, nghiêng
• Chụp cắt lớp vi tính ngực, bụng, chậu
• Chụp cộng hưởng từ (MRI) não
• Xạ hình xương
• Chụp PET toàn thân khi cần
b) Các chất chỉ điểm u (dấu hiệu sinh học bướu): giúp chẩn đoán xác định u nguyên phát tại phổi hay chẩn đoán phân biệt u di căn từ vị trí khác.
• Các chất chỉ điểm bướu giúp chẩn đoán xác định:
- SCC
- CEA
- Cyfra21-1
- ProGRP, NSE...
• Các chất chỉ điểm bướu giúp chẩn đoán phân biệt di căn phổi: CA 125, CA 15-3, CA 19-9, PSA,...
c) Các phương pháp lấy bệnh phẩm xác định chẩn đoán giải phẫu bệnh:
• Nội soi phế quản: chải rửa tế bào, sinh thiết u.
• Chọc hút chẩn đoán tế bào hoặc sinh thiết u, hạch trung thất dưới hướng dẫn siêu âm qua nội soi (EBUS: endoscopic bronchial ultrasound; EUS: endoscopic ultrasound)
• Chọc hút kim nhỏ chẩn đoán tế bào tế bào học (FNAC) hoặc sinh thiết lõi kim (score biopsy) u hoặc tổn thương di căn (trực tiếp hay dưới hướng dẫn siêu âm hoặc chụp cắt lớp điện toán)
• Cắt u hoặc sinh thiết qua phẫu thuật mở hoặc nội soi lồng ngực hoặc trung thất (VATS: video-assisted thoracoscopy; VAM: video-assisted mediastinoscopy)
d) Nội soi phế quản: để xác định chẩn đoán và đánh giá giai đoạn bệnh.
2.3. Chẩn đoán Tế bào học - Mô bệnh học - Sinh học phân tử
a) Chẩn đoán tế bào học:
• Bệnh phẩm tế bào học:
- Bệnh phẩm qua soi phế quản: rửa phế quản, rửa phế quản-phế nang, chải phế quản, chọc hút xuyên phế quản dưới hướng dẫn siêu âm (EBUS).
- Bệnh phẩm từ các dịch khoang cơ thể: dịch màng phổi, dịch màng tim, dịch màng bụng, dịch não tủy.
- Dịch chọc hút bằng kim nhỏ (FNA): chọc hút hạch bằng kim nhỏ, chọc hút mô mềm, chọc hút phổi bằng kim nhỏ, chọc hút các tổn thương di căn bằng kim nhỏ...
- Bệnh phẩm đờm.
• Chẩn đoán tế bào học: giúp chẩn đoán xác định và chẩn đoán loại tế bào học UTPKTBN.
b) Chẩn đoán mô bệnh học
• Bệnh phẩm mô bệnh học:
- Bệnh phẩm qua soi phế quản: sinh thiết phế quản, sinh thiết xuyên phế quản, sinh thiết dưới hướng dẫn siêu âm nội phế quản (EBUS).
- Bệnh phẩm sinh thiết u phổi hay sinh thiết phổi-màng phổi dưới chụp cắt lớp điện toán.
- Bệnh phẩm qua phẫu thuật lồng ngực: phẫu thuật ngực hở, phẫu thuật qua nội soi dưới màn hình video (VATs), nội soi trung thất.
- Bệnh phẩm qua sinh thiết màng phổi: sinh thiết màng phổi bằng kim (kim Abrams, kim Castelain...), sinh thiết màng phổi qua nội soi.
- Bệnh phẩm sinh thiết các tổn thương di căn: hạch lymphô, mô mềm thành ngực, mô mềm dưới da, mô xương...
- Đúc khối tế bào (Cell Block): dịch màng phổi, dịch màng tim.
• Chẩn đoán mô bệnh học: giúp chẩn đoán xác định và chẩn đoán loại mô học UTPKTBN.
c) Chẩn đoán sinh học phân tử:
• Bệnh phẩm sinh học phân tử:
- Các kỹ thuật chẩn đoán sinh học phân tử: đều thực hiện được trên các mẫu bệnh phẩm mô bệnh học và tế bào học.
- Ngoài ra, xét nghiệm sinh học phân tử còn thực hiện được trên mẫu bệnh phẩm huyết tương chủ yếu để phát hiện các đột biến EGFR mắc phải hay thứ phát sau khi được điều trị các thuốc kháng tyrosine kinase (TKIs), trong đó quan trọng nhất là đột biến T790M tại exon 20 của gen EGFR. Trong một số trường hợp mẫu bệnh phẩm mô bệnh học hay tế bào học không đủ số lượng tế bào để chẩn đoán sinh học phân tử, có thể dùng mẫu bệnh phẩm huyết tương để chẩn đoán đột biến EGFR.
• Các loại kỹ thuật đang được sử dụng trong chẩn đoán UTPKTBN: Giải trình tự gen trực tiếp: Sanger Sequensing, RealTime-PCR, ddPCR: PCR kỹ thuật số, Giải trình tự gen chọn lọc: Pyrosequensing, Giải trình tự gen thế hệ mới: Next Generation Sequensing.
• Các xét nghiệm sinh học phân tử (Molacular Pathology):
- Xét nghiệm chẩn đoán đột biến gen EGFR: sử dụng bằng nhiều phương pháp: giải trình tự gen trực tiếp Sanger, kỹ thuật RealTime-PCR, kỹ thuật PCR kỹ thuật số, giải trình tự gen chọn lọc Pyrosequensing, giải trình gen thế hệ mới.
- Xét nghiệm chẩn đoán các biểu hiện tái sắp xếp gen ALK và ROS1: chủ yếu dùng nhuộm lai ghép gen tại chỗ FISH và kỹ thuật hóa mô miễn dịch.
- Xét nghiệm chẩn đoán các điểm kiểm soát miễn dịch PD-1/PD-L1 trong điều trị miễn dịch: sử dụng kỹ thuật hóa mô miễn dịch với các dấu ấn sinh học đặc hiệu.
- Xét nghiệm chẩn đoán các loại đột biến gen khác: BRAF V600E, HER-2, MET, PIK3CA, KRAS .
d) Các hình thái mô học trong ung thư phổi không tế bào nhỏ: Phân loại mô học UTPKTBN chủ yếu dựa vào phân loại của Tổ chức Y tế thế giới năm 2015 (WHO 2015). Tuy nhiên, trong UTPKTBN có các loại mô học quan trọng cần chú ý:
• Ung thư biểu mô tuyến (Adenocarcinoma) với các phân nhóm mô học cần chú ý: ung thư biểu mô tuyến tại chỗ (AIS: Adenocarcinoma in situ); ung thư biểu mô tuyến xâm lấn tối thiểu (Minimally invasive adenocarcinoma); ung thư biểu mô tuyến xâm lấn (Invasive adenocarcinoma).
• Ung thư biểu mô tế bào vẩy (Squanous Cell Carcinoma).
• Ung thư biểu mô tuyến-vẩy (Adenosquamous carcinoma)
• Ung thư biểu mô tế bào lớn (Large Cell Carcinoma)
• Các bướu nội tiết thần kinh của phổi (Neuroendocrine Tumours).
• Ung thư biểu mô dạng sarcôm (Sarcomatoid Carcinoma).
Sơ đồ chẩn đoán
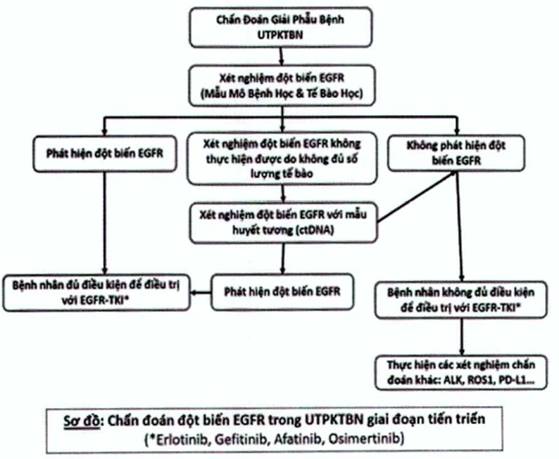
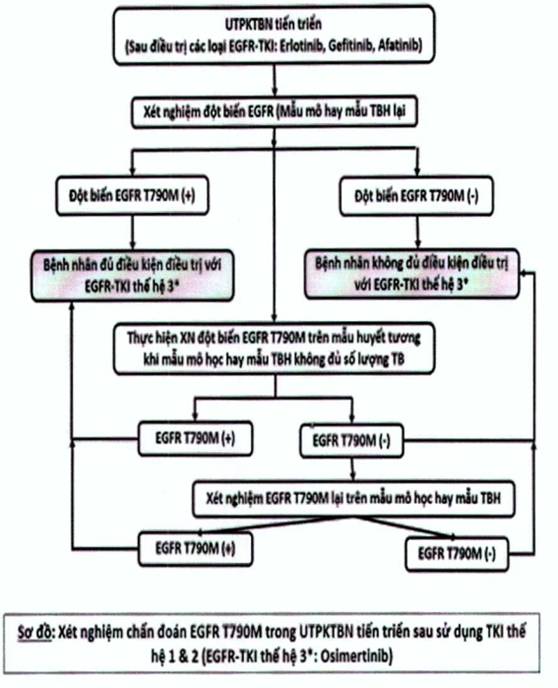
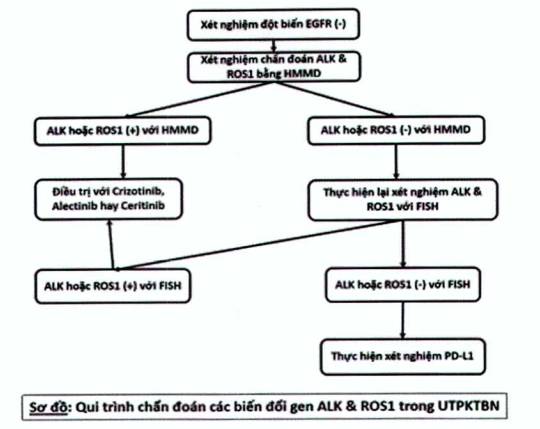
|
Kháng thể PDL-1 |
Hệ thống nhuộm |
Các thuốc miễn dịch |
Các trị số tính điểm biểu hiện PDL-1 |
|
28.8 |
Dako Link 48 |
Nivolumab |
≥ 1%, ≥ 5% |
|
22C3 |
Dako Link 48 |
Pembrolizumad |
≥ 1%, ≥ 50% |
|
SP142 |
Benchmark hay Ultra Ventana |
Atezolizumab |
Tế bào bướu ≥ 1%, ≥ 5%, ≥ 50% Tế bào miễn dịch ≥ 1 %, ≥ 5%, ≥ 10% |
|
SP263 |
Benchmark hay Ultra Ventana |
Durvalumab |
≥ 25% |
Bảng tóm tắt: Biểu hiện của các điểm ức chế miễn dịch PDL-1
2.4. Chẩn đoán xác định
a) Chẩn đoán xác định ung thư phổi phải dựa vào giải phẫu bệnh trong tình huống có thể thực hiện được. Chẩn đoán giải phẫu bệnh giúp xác định chính xác loại mô học và các dấu hiệu sinh học phân tử để định hướng điều trị chuẩn xác hơn.
b) Một số ung thư phổi giai đoạn sớm được phát hiện tình cờ hoặc tầm soát qua chụp cắt lớp điện toán lồng ngực biểu hiện dưới dạng nốt nhỏ cần được đánh giá và cân nhắc xử trí một cách thận trọng để tránh bỏ qua cơ hội điều trị khỏi cho một số bệnh nhân.
c) Chẩn đoán tổn thương phổi kích thước nhỏ: Các tổn thương nốt phổi có kích thước ≥ 8mm cần được lưu ý đánh giá và xử trí theo kích thước và nguy cơ ác tính theo khuyến cáo dưới đây:
Bảng: Đánh giá nguy cơ ác tính
|
Tiêu chuẩn đánh giá |
Nguy cơ ác tính |
||
|
Thấp (<5%) |
Vừa (5-65%) |
Cao (>65%) |
|
|
Lâm sàng |
Trẻ tuổi, hút thuốc ít, không tiền căn ung thư, kích thước lớn, bờ đều, và/hoặc vị trí ở ngoài thùy trên |
Có hỗn hợp các đặc điểm của nguy cơ thấp và cao |
Nhiều tuổi, hút thuốc, tiền căn mắc ung thư, kích thước lớn, bờ không đều/tua gai, và/hoặc vị trí ở thùy trên |
|
Kết quả FDG PET |
Chuyển hóa thấp |
Chuyển hóa trung bình hoặc yếu |
Chuyển hóa cao |
|
Kết quả sinh thiết ngoài phẫu thuật (soi phế quản, sinh thiết qua thành ngực) |
Lành tính |
Không xác định |
Nghi ngờ ác tính |
|
Kết quả theo dõi qua chụp điện toán cắt lớp |
Tổn thương tan hoàn toàn hoặc gần hoàn toàn, giảm kích thước dần hoặc không tăng kích thước trong thời gian theo dõi hơn 2 năm (nốt đặc) hoặc 3-5 năm (nốt hỗn hợp) |
Không áp dụng |
Nốt tăng kích thước rõ |
Sơ đồ xử trí tổn thương nốt phổi >8mm
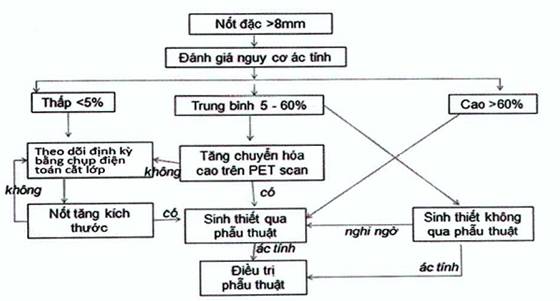
Các tổn thương nốt nhỏ dưới 8mm cũng cần được theo dõi định kỳ sát sao bằng chụp cắt lớp vi tính lồng ngực, từ mỗi 3 đến 12 tháng tùy theo ước lượng nguy cơ ác tính (lâm sàng, tính chất hình ảnh học của tổn thương...).
2.5. Chẩn đoán giai đoạn
Áp dụng theo bảng phân loại TNM8 do Hội Nghiên cứu Ung thư Phổi Thế giới (The International Association for the Study of Lung Cancer (IASLC) xây dựng:
Phân giai đoạn lâm sàng theo TNM
U nguyên phát (T)
|
T0 |
|
Không có u nguyên phát |
|
T1 |
|
Kích thước U ≤ 3cm, bao quanh bởi nhu mô hoặc màng phổi tạng, không dấu xâm lấn gần hơn cuống phổi thùy trên nội soi phế quản |
|
|
T1a |
Kích thước U ≤ 1cm |
|
|
T1b |
Kích thước U > 1cm nhưng ≤ 2cm |
|
|
T1c |
Kích thước U > 2cm nhưng ≤ 3cm |
|
T2 |
|
Kích thước U >3cm nhưng ≤ 5cm hoặc có bất kỳ đặc tính sau đây: xâm lấn màng phổi tạng, xâm lấn phế quản gốc cách carina xa hơn 2cm, xẹp/viêm phổi thùy nhưng không hết toàn bộ phổi. |
|
|
T2a |
Kích thước U >3cm nhưng ≤ 4cm |
|
|
T2b |
Kích thước U >4cm nhưng ≤ 5cm |
|
T3 |
|
Kích thước U > 5cm nhưng ≤ 7cm hoặc xâm lấn trực tiếp vào thành ngực, cơ hoành, thần kinh hoành, màng phổi trung thất, màng ngoài tim; hoặc bướu xâm lấn phế quản gốc cách carina gần hơn 2cm; hoặc xẹp phổi/viêm phổi tắc nghẽn toàn bộ một bên phổi; hoặc nốt di căn cùng thùy phổi. |
|
T4 |
|
Kích thước U >7cm hoặc bất kỳ kích thước xâm lấn vào tim, mạch máu lớn, khí quản, thần kinh hồi thanh quản, thực quản, thân đốt sống, carina; hoặc nốt di căn khác thủy cùng bên phổi. |
|
■ Hạch vùng (N) |
||
|
N0 |
|
Không di căn hạch vùng |
|
N1 |
|
Di căn hạch quanh phế quản, hạch rốn phổi, trong phổi cùng bên, kể cả do xâm lấn trực tiếp. |
|
N2 |
|
Di căn hạch trung thất cùng bên hoặc hạch dưới carena. |
|
■ Di căn xa (M) |
||
|
M0 |
|
Không di căn xa |
|
M1a |
|
Di căn thùy phổi đối bên, nốt màng phổi hoặc tràn dịch màng phổi |
|
M1b |
|
Di căn ngoài lồng ngực đơn ổ một vị trí |
|
M1c |
|
Di căn ngoài lồng ngực nhiều ổ một hoặc nhiều vị trí |
Việc phân giai đoạn lâm sàng rất quan trọng vì giúp xác định chiến lược điều trị và tiên lượng bệnh nhân.
Giai đoạn lâm sàng (theo IASLC lần thứ 8)
|
Không xác định u |
Tx |
N0 |
M0 |
|
Giai đoạn 0 |
Tis |
N0 |
M0 |
|
Giai đoạn I |
|
|
|
|
Giai đoạn IA1 |
T1a (mi) |
N0 |
M0 |
|
|
T1a |
N0 |
M0 |
|
Giai đoạn IA2 |
T1b |
N0 |
M0 |
|
Giai đoạn IA3 |
T1c |
N0 |
M0 |
|
Giai đoạn IB |
T2a |
N0 |
M0 |
|
Giai đoạn II |
|
|
|
|
Giai đoạn IIA |
T2b |
N0 |
M0 |
|
Giai đoạn IIB |
T1a-c |
N1 |
M0 |
|
|
T2a-b |
N1 |
M0 |
|
|
T3 |
N0 |
M0 |
|
Giai đoạn III |
|
|
|
|
Giai đoạn IIIA |
T1a-c |
N2 |
M0 |
|
|
T2a-b |
N2 |
M0 |
|
|
T3 |
N1 |
M0 |
|
|
T4 |
N0 |
M0 |
|
|
T4 |
N1 |
M0 |
|
Giai đoạn IIIB |
T1a-c |
N3 |
M0 |
|
|
T2a-b |
N3 |
M0 |
|
|
T3 |
N2 |
M0 |
|
|
T4 |
N2 |
M0 |
|
Giai đoạn IIIC |
T3 |
N3 |
M0 |
|
|
T4 |
N3 |
M0 |
|
Giai đoạn IV |
Bất kỳ T |
Bất kỳ N |
M1 |
|
Giai đoạn IVA |
Bất kỳ T |
Bất kỳ N |
M1a,b |
|
Giai đoạn IVB |
Bất kỳ T |
Bất kỳ N |
M1c |
3. ĐIỀU TRỊ
3.1. Nguyên tắc, mục tiêu điều trị
a) Nguyên tắc: Điều trị theo nguyên tắc cá thể hóa theo từng bệnh nhân, cần cân nhắc tất cả các yếu tố:
• Bệnh lý: thể mô bệnh học và sinh học phân tử, giai đoạn bệnh, diễn tiến sau các điều trị trước,...
• Bệnh nhân: thể trạng, tuổi, bệnh kết hợp, hoàn cảnh kinh tế - xã hội, nguyện vọng của bệnh nhân...
• Điều kiện trang thiết bị, nguồn lực của cơ sở y tế...
b) Mục tiêu điều trị: phân theo giai đoạn:
• Điều trị triệt căn nhằm mục tiêu chữa khỏi: giai đoạn sớm khu trú tại chỗ tại vùng (giai đoạn I, II, IIIA).
• Điều trị mang tính giảm nhẹ, tăng chất lượng cuộc sống và kéo dài thời gian sống còn áp dụng cho giai đoạn tiến triển tại chỗ-tại vùng hoặc tái phát di căn (giai đoạn IIIB, IIIC, lV).
Đối với giai đoạn còn khu trú, phẫu thuật và xạ trị là phương pháp điều trị mang tính triệt căn. Giai đoạn tiến triển (tái phát di căn) việc điều trị chủ yếu mang tính làm dịu triệu chứng và kéo dài thời gian sống còn. Giai đoạn tiến triển tại chỗ tại vùng hiện đang nghiên cứu áp dụng phương cách điều trị đa mô thức, trong đó phương thức hóa-xạ trị đồng thời được áp dụng nhiều nơi.
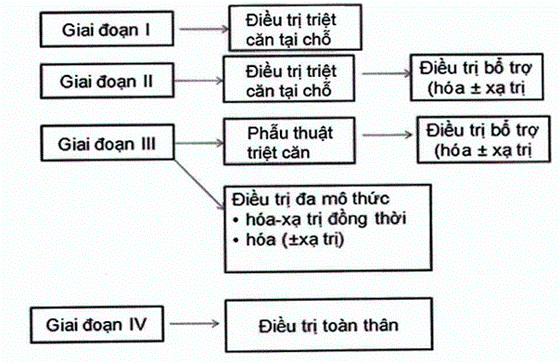
Sơ đồ điều trị ung thư phổi không tế bào nhỏ theo giai đoạn
3.2. Điều trị giai đoạn khu trú:
Giai đoạn khu trú: được xem như khi tổn thương còn mang tính khu trú tại chỗ, tại vùng gồm giai đoạn I và II. Phẫu thuật và xạ trị mang tính cách triệt để, vai trò của hóa trị bổ trợ trước và sau điều trị triệt để còn khiêm tốn.
a) Phẫu thuật: yêu cầu của phẫu thuật triệt để bao gồm việc cắt trọn thùy phổi mang khối u đạt diện cắt âm tính (không có tế bào bướu), lấy đi từ 16 - 20 hạch thuộc ít nhất 3 nhóm hạch (2 từ trung thất cùng và đối bên) và rửa màng phổi cùng bên. Đôi khi cần thiết phải cắt hai thùy kế cận hoặc một bên phổi. Nguy cơ tử vong vào khoảng 3% sau phẫu thuật cát thùy và 7% sau cắt một bên phổi.
Đối với các tổn thương nhỏ <3 cm ở ngoại biên với mô học là ung thư biểu mô tại chỗ (AIS) hoặc xâm lấn ít (MIA), phẫu thuật cắt hình chêm (wedge resection) với bờ diện cắt âm tính cũng cho kết quả sống còn lâu dài. Phẫu thuật cắt hình chêm cho các tổn thương trung tâm thường có nguy cơ tái phát tại chỗ cao hơn từ 3 đến 5 lần phẫu thuật cắt thùy.
Kỹ thuật phẫu thuật lồng ngực dưới sự trợ giúp của video (VATS) và cắt qua rôbốt: thường được áp dụng cho các tổn thương nhỏ và vừa ở ngoại biên, không hoặc ít hạch vùng. Đây là các kỹ thuật can thiệp ít xâm lấn với các ưu điểm thời gian nằm viện ngắn, ít đau sau mổ, bệnh nhân hồi phục nhanh nhưng cần chọn lọc bệnh nhân kỹ lưỡng hơn. VATS cho các kết quả sống còn và tỉ lệ tái phát thấp tương đương như phẫu thuật cắt thùy mở. Bệnh nhân có kết quả sống 5 năm từ 70 - 80% cho giai đoạn bệnh lý IA, 60% cho giai đoạn IB và 40 - 50% cho giai đoạn II. Bệnh nhân N2 (giai đoạn IIIA) khu trú một nhóm hạch cũng đạt tỷ lệ 25 - 30% sống 5 năm sau VATS. Tỉ lệ tái phát tại chỗ sau 5 năm cũng rất thấp với 5% cho giai đoạn T1 và 9% cho giai đoạn T2.
Kỹ thuật cắt qua rôbốt đang được nghiên cứu và cũng cho kết quả ban đầu hứa hẹn với ít di chứng và kết quả lâu dài về mặt ung bướu học tương đương.
• Hóa trị tân bổ trợ: hóa trị trước mổ cho các ung thư phổi giai đoạn còn khu trú nhằm hai mục đích: tiêu diệt các di căn vi thể đã có và giảm kích thước tổn thương tạo thuận lợi cho phẫu thuật tiếp theo. Hóa trị tân bổ trợ là lựa chọn tiêu chuẩn trong điều trị giai đoạn IIIA, vai trò chưa được xác định rõ trong các giai đoạn sớm hơn.
• Hóa trị bổ trợ: sau mổ đã được nghiên cứu nhiều và các nghiên cứu cho kết quả khác nhau. Hóa trị bổ trợ hiện được chỉ định sau phẫu thuật cho các trường hợp có giai đoạn từ IB trở lên. Hóa trị hỗ trợ thường được thực hiện 4 chu kỳ với phối hợp thuốc có platin (cisplatin được ưu tiên chọn lựa so với carboplatin)
• Xạ trị bổ trợ: xạ trị bổ trợ sau mổ các trường hợp ung thư phổi giai đoạn sớm cũng đã được nghiên cứu và cũng còn nhiều bàn cãi. Xạ trị bổ trợ sau phẫu thuật giai đoạn I và II không được xác nhận có ích lợi. Trong thực hành lâm sàng, xạ trị bổ trợ thường được chỉ định sau mổ cho một số trường hợp có yếu tố nguy cơ cao tái phát tại chỗ tại vùng như:
- Xâm lấn trung thất
- Di căn nhiều hạch hay nhiều nhóm hạch
- Xâm lấn vỡ vỏ bao hạch
- Hạch di căn có kích thước lớn
- Bờ diện cắt xâm lấn đại thể
- Bờ diện cắt còn tế bào ung thư
Liều xạ trị thường dùng 54Gy phân bố qua 27 - 30 phân liều. Trong trường hợp điều trị bổ trợ bao gồm cả hóa và xạ trị thì xạ trị được tiến hành sau hóa trị.
b) Điều trị các trường hợp không phẫu thuật được: một số trường hợp bệnh nhân ung thư phổi giai đoạn khu trú nhưng không thể tiến hành phẫu thuật triệt căn do nguy cơ phẫu thuật cao, có thể cân nhắc áp dụng một số biện pháp điều trị khác.
• Xạ trị triệt căn: xạ trị triệt căn là một lựa chọn thay thế cho các tổn thương còn khu trú và có thể tiến hành theo kỹ thuật xạ trị quy ước hoặc xạ trị định vị thân (SBRT: stereostatic body radiotherapy).
- Xạ trị quy ước: thường với liều xạ trị mỗi ngày (2Gy cho mỗi phân liều) trong 5 ngày mỗi tuần, với tổng liều ít khi vượt quá 70Gy. Tỉ lệ kiểm soát bướu vào khoảng 50%.
- Xạ trị định vị thân SBRT mới được phát triển nghiên cứu và chưa phải là khuyến cáo thường quy. Kỹ thuật xạ trị nhầm đưa một liều chiếu xạ cao vào vị trí chính xác qua một số ít phân liều (3 -5 lần chiếu xạ) nhằm đạt liều tương đương sinh học (biologically equivalent doses -BEDs) cao hơn 100 Gy trong thời gian ngắn 1 - 2 tuần, hiệu quả kiểm soát bướu tại chỗ lên tới 85% - 90%.
Kỹ thuật SBRT với liều 18 - 20Gy mỗi phân liều an toàn và hiệu quả cho các tổn thương ngoại biên nhưng thường kèm theo tác dụng phụ nặng độ 3 khi dùng cho các tổn thương trung tâm. Liều thích hợp hay được khuyến cáo sử dụng là 10 - 12Gy mỗi lần trong 3 hoặc 4 phân liều.
Sơ đồ tóm tắt xử trí ung thư phổi không tế bào nhỏ giai đoạn I
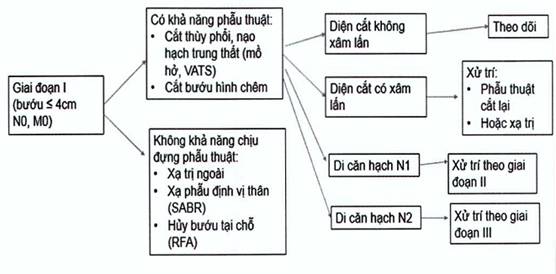
Sơ đồ xử trí ung thư phổi không tế bào nhỏ giai đoạn I
Sơ đồ tóm tắt xử trí ung thư phổi không tế bào nhỏ giai đoạn II
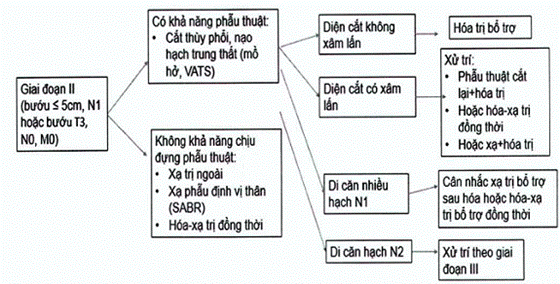
Sơ đồ xử trí ung thư phổi không tế bào nhỏ giai đoạn II
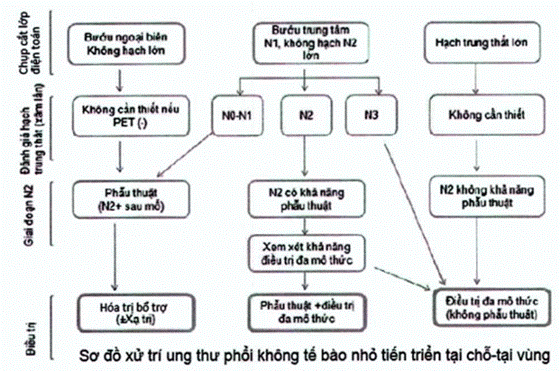
3.3. Điều trị giai đoạn tiến triển tại chỗ (IIIA/IIIB)
Điều trị giai đoạn này thường được cá thể hóa theo từng trường hợp bệnh nhân cụ thể với nhiều mô thức áp dụng lần lượt hoặc đồng thời.
a) Xạ trị: xạ trị có thời được coi là mô thức điều trị chuẩn cho ung thư phổi không tế bào nhỏ tiến xa tại chỗ (IIIA/IIIB) nhưng kết quả kiểm soát tại chỗ thường kém và tỷ lệ sống còn thấp.
Xạ trị tăng phân liều (CHART) có vẻ cải thiện kết quả sống còn, nhất là khi phối hợp với hóa trị. Nhiều nghiên cứu cải tiến kỹ thuật nhằm tăng liều xạ vào bướu đồng thời giảm độc tính mô chung quanh.
b) Phối hợp hóa và xạ trị đồng thời:
• Hiện tại, hóa-xạ trị đồng thời được khuyến cáo như một xử trí tiêu chuẩn cho bệnh nhân ung thư phổi không tế bào nhỏ giai đoạn III (không phẫu thuật được) có chỉ số hoạt động cơ thể ECOG 0/1 và không bị giảm hơn 5% trọng lượng cơ thể. Kỹ thuật xạ trị bao gồm xạ trị một phân liều mỗi ngày, tổng liều 74Gy thường kèm theo kết quả sống còn thấp hơn 60Gy. Hóa trị kèm theo thường là platin hoặc bộ đôi platin với các thuốc thế hệ III như taxane, vinorelbine ... Các thuốc nhắm trúng đích mới (cetuximab, gefitinib...) hiện chưa xác định được vai trò trong phối hợp với xạ trị.
• Một phân tích gộp cho thấy hóa-xạ trị đồng thời có hiệu quả cải thiện kết quả sống còn cho bệnh nhân ung thư phổi không tế bào nhỏ tiến xa tại chỗ chủ yếu nhờ vào việc giảm tỷ lệ tiến triển tại chỗ tại vùng. Ích lợi sống còn tuyệt đối trong 3 năm là 6%. Tuy nhiên hóa-xạ trị đồng thời tăng nguy cơ độc tính viêm thực quản, viêm phổi...
3.4. Điều trị giai đoạn tiến triển (tái phát/di căn):
Trong giai đoạn tiến xa, mục đích điều trị là để giảm thiểu triệu chứng liên quan bệnh, cải thiện chất lượng cuộc sống và kéo dài thời gian sống thêm. Phương pháp điều trị đặc hiệu chủ yếu dùng trong giai đoạn này là các biện pháp điều trị mang tính toàn thân bao gồm hóa trị bằng các thuốc gây độc tế bào, điều trị nhắm trúng đích, điều trị miễn dịch... Các biện pháp xử trí tại chỗ tại vùng như phẫu thuật, xạ trị cũng được cân nhắc áp dụng tùy tình hình cụ thể của từng bệnh nhân.
Hướng xử trí ung thư phổi không tế bào nhỏ giai đoạn tiến triển có thể tóm tắt theo sơ đồ dưới đây (theo dạng mô học ung thư biểu mô tế bào vẩy và khác vẩy):
Sơ đồ xử trí ung thư phổi tế bào vẩy giai đoạn tiến triển:
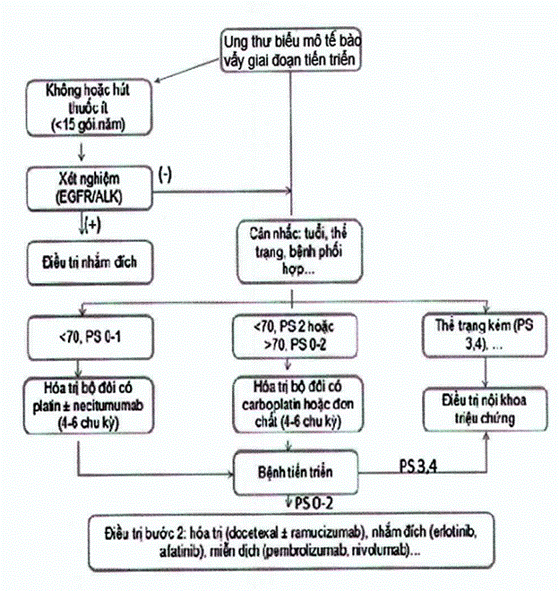
Sơ đồ xử trí ung thư phổi loại không tế bào vẩy giai đoạn tiến triển

a) Bệnh nhân có đột biến EGFR dạng hoạt động:
• Đa số các đột biến gen EGFR ở dạng hoạt động, thường gặp nhất là các đột biến mất đoạn exon 19, đột biến điểm L851R,...
• Điều trị bước một có thể chọn lựa một trong các thuốc ức chế EGFR tyrosin kinase thế hệ I hoặc II gồm:
- Gefitinib 250mg/ngày
- Erlotinib 150 mg/ngày
- Afatinib 40mg/ngày
- Osimertinib 80mg/ngày
• Thuốc được dùng kéo dài cho đến khi bệnh tiến triển. Trong trường hợp này bệnh nhân cần được xét nghiệm tìm đột biến kháng thuốc mắc phải T790M qua các xét nghiệm sinh học phân tử. Bệnh nhân có đột biến T790M cần được điều trị bằng thuốc ức chế EGFR tyrosin kinase thế hệ III osimertinib.
b) Bệnh nhân có đột biến dạng tái sắp xếp ALK:
Điều trị bước một: crizotinib, ceritinib hoặc alectinib
c) Các đột biến hiếm gặp: điều trị theo đích phân tử đặc hiệu (phần phụ lục): Bệnh nhân không có các đột biến đích và có tăng biểu hiệu PD L1 >50% có thể được điều trị bước một với thuốc ức chế điểm kiểm soát miễn dịch pembrolizumab
d) Bệnh nhân không có các đột biến đích:
• Điều trị đặc hiệu toàn thân dựa vào hóa trị bộ đôi có platin, phân theo hai nhóm lớn là ung thư biểu mô tế bào vẩy và không vẩy (phần phụ lục).
• Nhóm tế bào vẩy không sử dụng pemetrexed, bevacizumab
• Nhóm không tế bào vẩy cân nhắc phối hợp thêm bevacizumab với hóa trị theo các yếu tố lâm sàng và hình ảnh như: bướu ở vị trí ngoại biên, không triệu chứng ho ra máu, không hình ảnh phá hủy hang trung tâm, không xâm lấn mạch máu lớn.
3.5. Điều trị các tình huống đặc biệt:
a) Di căn xương: xử trí bao gồm:
• Điều trị đặc hiệu toàn thân
• Điều trị triệu chứng hướng xương: acid zoledronic 4mg truyền tĩnh mạch mỗi 2-4 tuần.
• Điều trị tăng cường tại chỗ: xạ trị tại chỗ hoặc dược chất phóng xạ toàn thân.
• Các biện pháp phẫu thuật thần kinh, chỉnh hình nhằm cố định xương hoặc giải áp chèn ép tủy...
b) Di căn não: xử trí bao gồm:
• Điều trị đặc hiệu toàn thân
• Điều trị triệu chứng: chống phù não, chống động kinh ...
• Điều trị tăng cường tại chỗ: xạ phẫu (dao gamma quay) có hoặc không phối hợp xạ trị toàn bộ não (20Gy/5 phân liều hoặc 30Gy/ 10 phân liều), trong đó xạ trị toàn bộ não là quan trọng trong tình huống di căn não nhiều ổ.
4. THEO DÕI SAU ĐIỀU TRỊ: Lịch trình theo dõi và xét nghiệm đánh giá thay đổi tùy theo bệnh cảnh lâm sàng.
4.1. Giai đoạn sớm: theo dõi tái phát, di căn và xử trí các tác dụng phụ của điều trị (phẫu thuật, xạ trị, hóa trị bổ trợ):
• Lịch trình: mỗi 2 tháng/1 lần trong năm đầu, mỗi 3 tháng/1 lần trong 2 năm sau, mỗi 6 tháng/lần từ năm thứ tư.
• Phương tiện đánh giá: khám lâm sàng, X quang, chụp cắt lớp vi tính,...
4.2. Giai đoạn tiến xa tại chỗ tại vùng: theo dõi bệnh tiến triển, di căn và xử trí các tác dụng phụ của điều trị (phẫu thuật, xạ trị, hóa trị).
• Lịch trình: mỗi 2 tháng/ năm đầu, mỗi 3 tháng/1 lần trong các năm sau.
• Phương tiện đánh giá: khám lâm sàng, X quang, chụp cắt lớp vi tính,...
4.3. Giai đoạn tiến xa, di căn: theo dõi bệnh tiến triển, di căn mới và xử trí các tác dụng phụ của điều trị (phẫu thuật, xạ trị, hóa trị, điều trị đích).
• Lịch trình: mỗi tháng/1 lần trong năm đầu, mỗi 2 tháng/1 lần trong các năm sau.
• Phương tiện đánh giá: khám lâm sàng, X quang, chụp cắt lớp vi tính ...
5. TIÊN LƯỢNG
Các yếu tố tiên lượng quan trọng gồm:
• Giai đoạn: yếu tố tiên lượng quan trọng nhất. Giai đoạn I và II phẫu thuật được có tiên lượng sống 5 năm từ 50 - 80%, giai đoạn III tỉ lệ này giảm xuống còn từ 20 - 40%. Riêng giai đoạn IV tỉ lệ sống 5 năm rất thấp (<5%)
• Chỉ số hoạt động cơ thể: có ý nghĩa rất quan trọng trong giai đoạn tiến xa
• Một số yếu tố tiên lượng xấu: sụt cân (>10% trọng lượng cơ thể trong vòng 3 tháng) bạch cầu hạt tăng cao
• Yếu tố sinh học phân tử:
- Tiên lượng xấu: đột biến K-ras, tăng biểu hiện EGFR (c-erbB-1),VEGF), c-Met đột biến p53...
- Tiên lượng tốt: đột biến hoạt hóa EGFR...
6. TẦM SOÁT VÀ DỰ PHÒNG
6.1. Tầm soát: Chụp cắt lớp điện toán xoắn ốc năng lượng thấp (liều 1,5 mSv so với 8 mSv cho chụp cắt lớp điện toán lồng ngực thường quy) có thể được sử dụng để tầm soát phát hiện sớm các tổn thương nhỏ ở phổi trên đối tượng người có nguy cơ cao mắc ung thư phổi (lớn tuổi, tiền căn hút thuốc hơn 30 gói.năm).
6.2. Dự phòng: Biện pháp phòng ngừa hữu hiệu nhất là phòng chống tác hại của thuốc lá.
Tài liệu tham khảo
1) IARC. World Cancer Report 2014
2) UICC Manual of Clinical Oncology 8th Ed 2004
3) American Cancer Society Textbook of Clinical Oncology. 2nd Ed. 1995
4) Textbook of Lung Cancer. Hein Hansen 2008
5) Cancer: Principles and Practice of Oncology. De Vita. 9th Ed. 2014
6) Ung thư học lâm sàng, Nguyễn Chấn Hùng. Tập 2
7) Evaluation of Individuals With Pulmonary Nodules: When Is It Lung Cancer? Diagnosis and Management of Lung Cancer, 3rd ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. CHEST 2013; 143(5)(Suppl): e93S-e120S
8) Evaluation of Pulmonary Nodules Clinical Practice Consensus Guidelines for Asia. CHEST 2016; 150(4): 877-893
9) Non-Small Cell Lung Cancer - NCCN Guidelines Version 3.2018, 17-32.
10) Second ESMO consensus conference on lung cancer: pathology and molecular biomarkers for non-small-cell lung cancer; Annals of Oncology, 1681-1690, 2014, Published online 8 April 2014.
11) The role of the Pathologist in the diagnosis and biomarker profiling of Lung Cancer; Keith M Kerr et.al.; Preceptorship Lung Cancer 2018 - ESMO; Annals of Oncology, 1798-1801, 2018, Published online 3 March 2018.
12) Updated Molecular Testing Guideline for the Selection of Lung Cancer Patients for Treatment With Targeted Tyrosine Kinase Inhibitors - Guideline From the College of American Pathologists, the International Association for the Study of Lung Cancer, and the Association for Molecular Pathology; Journal of Thoracic Oncology Vol. 13 No. 3: 323-358.
13) Australian recommendations for EGFR T790M testingin advanced non-small cell lung cancer; Thomas JOHN, Jeffrey J BOWDEN, et al.; Asia-Pacifc Journal of Clinical Oncology 2017; Volume 5, April 2017, 1-15.
14) WHO Classification of Tumours of The Lung, Pleura & Thymus and Heart, Lyon 2015, International Agency for Research on Cancer, IARC Library Cataloguing in Publication Data, 5-68.
15) Metastatic non-small-cell lung cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology 27 (Supplement 5): v1-v27, 2016
16) Early and locally advanced non-small-cell lung cancer (NSCLC): ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology 28 (Supplement 4): iv1-iv21, 2017
PHỤ LỤC:
CÁC PHỐI HỢP ĐIỀU TRỊ TOÀN THÂN UNG THƯ PHỔI KHÔNG TẾ BÀO NHỎ
1. Hóa trị tân bổ trợ hoặc bổ trợ:
• Cisplatin 50 mg/m2 ngày 1 và 8, vinorelbine 25 mg/m2 ngày 1,8, 15, 22; chu kỳ mỗi 28 ngày x 4 chu kỳ.
• Cisplatin 100 mg/m2 ngày 1, vinorelbine 30 mg/m2 ngày 1,8, 15, 22; chu kỳ mỗi 28 ngày x 4 chu kỳ.
• Cisplatin 75-80 mg/m2 ngày 1, vinorelbine 25-30 mg/m2 ngày 1+8, chu kỳ mỗi 21 ngày x 4 chu kỳ.
• Cisplatin 100 mg/m2 ngày 1, etoposide 100 mg/m2 ngày 1-3; chu kỳ mỗi 28 ngày x 4 chu kỳ.
• Cisplatin 75 mg/m2 ngày 1, gemcitabine 1250 mg/m2 ngày 1, 8; chu kỳ mỗi 21 ngày x 4 chu kỳ.
• Cisplatin 75 mg/m2 ngày 1, docetaxel 75 mg/m2 ngày 1; chu kỳ mỗi 18 ngày x 4 chu kỳ.
• Cisplatin 75 mg/m2 ngày 1, pemetrexed 500 mg/m2 ngày 1; chu kỳ mỗi 18 ngày x 4 chu kỳ (không phải tế bào vẩy).
Các phối hợp thay thế cho bệnh nhân dung nạp kém cisplatin:
• Carboplatin AUC 6 ngày 1, paclitaxel 200 mg/m2 ngày 1, chu kỳ mỗi 21 ngày x 4 chu kỳ.
• Carboplatin AUC 5 ngày 1, gemcitabine 1000 mg/m2 ngày 1, 8; chu kỳ mỗi 21 ngày x 4 chu kỳ.
• Carboplatin AUC 5 ngày 1, pemetrexed 500 mg/m2 ngày 1, chu kỳ mỗi 21 ngày x 4 chu kỳ (không phải tế bào vẩy).
2. Hóa trị phối hợp đồng thời với xạ trị
• Cisplatin 50 mg/m2 ngày 1, 8, 29 và 36; etoposide 50 mg/m2 ngày 1-5, 29-33; phối hợp đồng thời với xạ trị.
• Cisplatin 100 mg/m2 ngày 1 và 29; Vinblastine 5 mg/m2/tuần x 5; phối hợp đồng thời với xạ trị.
• Carboplatin AUC 5 ngày 1; pemetrexed 500 mg/m2 ngày 1; chu kỳ mỗi 21 ngày x 4 chu kỳ; phối hợp đồng thời với xạ trị (không tế bào vẩy).
• Cisplatin 75 mg/m2 ngày 1; pemetrexed 500 mg/m2 ngày 1; chu kỳ mỗi 21 ngày X 3 chu kỳ; phối hợp đồng thời với xạ trị (không tế bào vẩy).(± duy trì thêm 4 chu kỳ pemetrexed 500 mg/m2).
• Paclitaxel 45-50 mg/m2 mỗi tuần, carboplatin AUC 2, phối hợp đồng thời với xạ trị (không tế bào vẩy).(± duy trì thêm 2 chu kỳ paclitaxel 200 mg/m2 và carboplatin AUC 6).
3. Hóa trị củng cố sau hóa-xạ trị đồng thời (giai đoạn III, không tiến triển bệnh sau 2 chu kỳ hóa-xạ trị đồng thời)
• Durvalumab 10 mg/kg IV mỗi 2 tuần cho đến 12 tháng.
4. Điều trị toàn thân giai đoạn tiến xa (tái phát/di căn)
4.1. Điều trị theo các đích đặc hiệu
|
|
Bước một |
Bước sau |
|
• Đột biến EGFR dạng hoạt động |
- Afatinib - Erlotinib - Gefitinib - Osimertinib |
- Osimertinib |
|
• Tái sắp xếp ALK |
- Alectinib - Ceritinib - Crizotinib |
- Alectinib - Brigatinib - Ceritinib |
|
• Tái sắp xếp ROSI |
- Ceritinib - Crizotinib |
- |
|
• Đột biến V600E |
- Dabrafenib/Trametinib |
- Dabrafenib/Trametinib |
|
• Tăng biểu hiện PD-L1 |
- Pembrolizumab |
- Atezolizumab - Nivolumab - Pembrolizumab |
4.2. Hóa trị
|
Ung thư biểu mô tuyến, ung thư biểu mô tế bào lớn, ung thư biểu mô không xếp loại (thể trạng tốt) |
|
|
• Bevacizumab/carboplatin/paclitaxel |
• Carboplatin/pemetrexed |
|
• Bevacizumab/carboplatin/pemetrexed |
• Cisplatin/docetaxel |
|
• Bevacizumab/cisplatin/pemetrexed |
• Cisplatin/etoposide |
|
• Carboplatin/albumin-bound paclitaxel |
• Cisplatin/gemcitabine |
|
• Carboplatin/docetaxel |
• Cisplatin/paclitaxel |
|
• Carboplatin/etoposide |
• Cisplatin/pemetrexed |
|
• Carboplatin/gemcitabine |
• Gemcitabine/docetaxel |
|
• Carboplatin/paclitaxel |
• Gemcitabine/vinorelbine • Pembrolizumab/carboplatin/pemetrexed |
|
Ung thư biểu mô tuyến, ung thư biểu mô tế bào lớn, ung thư biểu mô không xếp loại (thể trạng kém) |
|
|
• Albumin-bound paclitaxel • Carboplatin/albumin-bound paclitaxel • Carboplatin/docetaxel • Carboplatin/etoposide • Carboplatin/gemcitabine • Carboplatin/paclitaxel |
• Carboplatin/pemetrexed • Docetaxel • Gemcitabine • Gemcitabine/docetaxel • Gemcitabine/vinorelbinepaclitaxel • Pemetrexed |
|
Ung thư biểu mô tế bào vẩy (thể trạng tốt) |
|
|
• Carboplatin/albumin-bound paclitaxel • Carboplatin/docetaxel • Carboplatin/gemcitabine • Carboplatin/paclitaxel • Cisplatin/docetaxel |
• Cisplatin/etoposide • Cisplatin/gemcitabine • Cisplatin/paclitaxel • Gemcitabine/docetaxel • Gemcitabine/vinorelbine |
|
Ung thư biểu mô tế bào vẩy (thể trạng kém) |
|
|
• Albumin-bound paclitaxel • Carboplatin/albumin-bound paclitaxel • Carboplatin/docetaxel • Carboplatin/etoposide • Carboplatin/gemcitabine • Carboplatin/paclitaxel |
• Docetaxel • Gemcitabne • Gemcitabine/docetaxel • Gemcitabine/vinorelbine • Paclitaxel |


