Nội dung toàn văn Tiêu chuẩn Việt Nam TCVN 5156:1990 về thịt và sản phẩm của thịt - phương pháp phát hiện và đếm số Staphylococcus Aureus do Ủy ban Khoa học Nhà nước ban hành
TIÊU CHUẨN VIỆT NAM
TCVN 5156:1990
THỊT VÀ SẢN PHẨM CỦA THỊT
PHƯƠNG PHÁP PHÁT HIỆN VÀ ĐẾM SỐ STAPHYLOCOCCUS AUREUS
Meat and meat products
Detection and enumeration of Staphylococcus aureus
Trên cơ sở tiêu chuẩn TCVN 4830-89 hướng dẫn cibm về Staphylococcus aureus. Tiêu chuẩn này quy định phương pháp phát hiện và đếm số Staphylococcus aureus trong 1 gam thịt và trên 100 cm2 thịt và các sản phẩm của thịt dùng làm thực phẩm cho người và thức ăn gia súc.
1. Đặc tính chung
Vi khuẩn hình tròn, gram dương, kích thước 0,5 x 1 micrô mét, không có giáp mô, không có nha bào, không di động, tụ thành chùm nho hoặc ghép đôi, hợp thành chuỗi ngắn. Sinh trưởng trong môi trường hiếm khí, yếm khí có 7,5% muối; phân giải đường glucose và mannit, đóng vón huyết tương, tan hồng cầu, sắc tố màu vàng.
2. Nguyên tắc
Căn cứ vào đặc tính sinh hoá để xác định vi khuẩn. Pha loãng mẫu thử các đậm độ khác nhau, ria cấy trên môi trường chọn lọc để đếm và tính số vi khuẩn.
3. Lấy mẫu: Theo TCVN 5153-90.
4. Thiết bị và dụng cụ: Theo TCVN 5153-90.
5. Môi trường, huyết tương:
5.1. Phải dùng các loại hoá chất tinh khiết phân tích, nên sử dụng các thành phần cơ bản hoặc đã chế sẵn; khi dùng phải theo chỉ dẫn của nơi sản xuất. Môi trường phải bảo quản ở nơi tối, nhiệt độ 4 oC, không quá 1 tháng. Định kỳ kiểm tra lại môi trường bằng giống vi khuẩn tiêu chuẩn.
5.2. Môi trường, huyết tương (phụ lục B)
5.2.1. Môi trường thạch telurit - glycin (môi trường thạch T.G).
5.2.2. Môi trường nước thịt.
5.2.3. Môi trường nước thịt B.H.I.
5.2.4. Môi trường Chapman.
5.2.5. Dung dịch chống máu đông.
5.2.6. Huyết tương. Khi cùng huyết tương đông khô phải theo đúng chỉ dẫn của nơi sản xuất. Nếu chế huyết tương thì lấy máu thỏ cho vào bình đựng sẵn dung dịch chống đông theo tỷ lệ 9 phần máu một phần dung dịch ngăn máu đông; ly tâm 15-20 phút để hồng cầu lắng xuống đáy ống nghiệm, thu khối nước trong màu vàng nhạt (huyết tương).
Cũng như môi trường, trước khi dùng phải kiểm tra lại hiệu lực bằng chủng Step. aureus tiêu chuẩn.
6. Cách tiến hành
6.1. Yêu cầu cibm: Các dụng cụ, môi trường, v.v... và thao tác phải vô khuẩn.
6.2. Chuẩn bị mẫu thử: Thịt lạnh đông phải giải đông tự nhiên ở nhiệt độ trong phòng cho đến khi đạt 13 - 15oC, đồ hộp phải cọ rửa sạch vỏ ngoài, lau khô, ủ 37oC từ 5 - 7 ngày.
6.3. Chế huyền phù ban đầu.
6.3.1. Đếm số vi khuẩn trong 1 gam sản phẩm: cân 100 - 225 gam (không lấy mỡ, lấy cả chất lỏng nếu có) nghiền trước trong cối sứ, nghiền nhuyễn tiếp trong máy xay thịt từ 2 - 3 phút với tốc độ 10.000 vòng/phút, vừa nghiền vừa bổ sung dần 9 phần môi trường nước thịt hoặc B.H.I (10 -1)
6.3.2. Đếm số vi khuẩn trên 100 cm2 sản phẩm: Dùng những miếng giấy thấm vô khuẩn có kích thước 5 x 5 cm đã được làm ướt bằng nước muối đẳng trương, rồi dán lên bề mặt sản phẩm ở các vị trí khác nhau từ 4 - 8 miếng (100 - 200 cm2). Sau 2 phút chuyển toàn bộ giấy thấm vào bình đã đựng sẵn 10 - 20 ml môi trường nước thịt hoặc nước thịt B.H.I. và 10 - 15 viên bi thuỷ tinh. Lắc cho tan giấy, tuỳ theo khối lượng mẫu thử cần sử dụng mà pha loãng thành 1:1 (1ml tương đương với 1 cm2)
6.4. Đếm số vi khuẩn: Từ huyền phù ban đầu 6.3 tiếp tục pha loãng 10 lần (10-1, 10-2, 10-3 ...) (tùy mức nhiễm khuẩn mà quyết định). Mỗi đậm độ cấy vào 2 đĩa môi trường thạch Telurit - glycin một khối lượng bằng nhau trong khoảng từ 0,1 - 1 ml (tùy mức nhiễm khuẩn mà quyết định), dàn đều trên mặt thạch hoặc trộn đều trong thạch nóng lỏng ở 45oC, đặt úp đĩa môi trường, ủ 37 oC từ 24 - 48 giờ, đọc kết quả.
Khuẩn lạc Stap. aureus tròn, mặt nhẵn, viền mép gọn, màu đen, có vòng bao quanh màu trắng đục, sau 48 giờ chuyển thành vòng trắng rộng khoảng 3 mm, còn các tụ cầu khuẩn khác màu xám nhạt.
Căn cứ vào hình dạng và màu sắc trên mà đếm. Nếu nghi ngờ thì phân thành 2 nhóm: điển hình và không điển hình; chọn trong mỗi nhóm 5 khuẩn lạc để giám định phản ứng đông vón tuyết tương mà xác định tỷ lệ (theo phụ lục B, TCVN 5155-90).
6.5. Giám định tính chất sinh hoá:
6.5.1. Trên môi trường Chapman: Cấy (6.4) vào 2 đĩa môi trường, ủ 37oC trong 24 giờ, đọc kết quả.
Khuẩn lạc Stap. aureus tròn, hơi đục, mặt nhẵn, viền mép gọn, màu vàng.
6.5.2. Thử phản ứng đông vón trên phiến kính: Nhỏ 1 giọt nước muối lên phiến kính, dùng que cấy lấy vi khuẩn vừa đủ (6.4) trộn thành huyền dịch đục đều, nhỏ tiếp 1 giọt huyết tương vào và thêm thí nghiệm đối chứng âm tính (1 giọt nước muối và 1 giọt huyết tương). Đọc kết quả bằng kính lúp hoặc kính hiển vi.
6.5.3. Thử phản ứng đông vón trong ống nghiệm: Chỉ làm khi
6.5.2. âm tính. Cấy vi khuẩn ở 6.4. vào môi trường nước thịt B. H.I , ủ 37oC từ 20 - 24 giờ. Sau chuyển 0,1 ml canh khuẩn vào ống nghiệm cỡ 10 x 75 mm đã chứa sẵn 0,3 ml huyết tương pha loãng theo tỷ lệ 1 phần huyết tương, 3 phần nước. Làm thêm thí nghiệm đối chứng âm tính (0,1ml nước muối và 0,3 ml huyết tương pha loãng) trộn đều, ủ 37oC; đọc kết quả sau 2, 4, 6, 8 và 24 giờ.
Chú thích: Nếu dùng huyết tương đông khô thương phẩm thì theo hướng dẫn của nơi sản xuất
7. Tính toán kết quả
7.1. Căn cứ vào kết quả giám định tính chất sinh hoá
7.2. Căn cứ vào công thức dưới đây để tính số Staphylococcus aureus trong 1 gam hoặc trên 100 cm2 sản phẩm (theo phụ lục B, TCVN 5155-90)
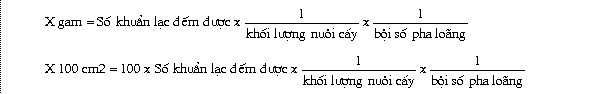
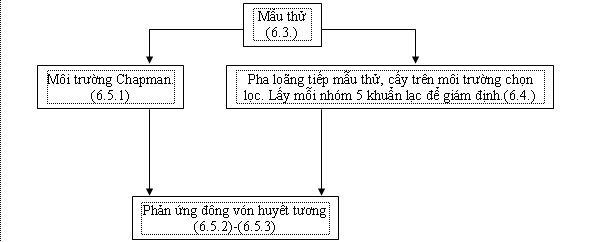
PHỤ LỤC A
PHÁC ĐỒ KIỂM NGHIỆM
PHỤ LỤC B
PHA CHẾ MÔI TRƯỜNG
B1. Môi trường thạch Telurit - glycin ( thạch T.G.).
B1.1. Môi trường cơ bản:
|
- Trypton |
10g |
|
- Bột cao thịt |
5g |
|
- Chất triết men (yeast extract) |
5g |
|
- Glycin |
12g |
|
- Lithium clorua |
5g |
|
- Mannit |
20g |
|
- Thạch |
18 - 20g |
|
- Nước cất |
1.000ml |
|
- Nếu cần thì cho thêm dung dịch sulfamezatin |
27,5ml |
Hoà tan các thành phần trên trong nước sôi. Chỉnh pH 7,4 - 7,6. Hấp 115oC trong 15 phút.
Chú thích
1/ Có thể thay 1000 ml nước cất và 5g bột cao thịt bằng 1000 ml nước thịt.
2/ Dung dịch Sulfamezatin (dùng khi mẫu thử nghi có vi khuẩn Proteus):
- Sulfamezatin 0,2g
- Natrihydroxyt, dung dịch 0,1N 10 ml
- Nước cất vừa đủ 100 ml
Hoà tan Sulfamezatin trong dung dịch Natrihydroxyt. Cho thêm nước cất vừa đủ 100 m.
B1.2. Dung dịch Telurit:
- Kali telurit 1g
- Nước cất 100ml
Hoà tan trong nước đun nóng. Lọc vô khuẩn. Bảo quản 0 - 4oC.
B1.3. Dung dịch Natri pyruvat:
- Natri pyruvat 20 g
- Nước cất 100 ml
Hoà tan trong nước đun nóng. Lọc vô khuẩn. Bảo quản 0 - 4oC.
B1.4. Môi trường hoàn chỉnh:
- Môi trường cơ bản (B1.1) 94 ml
- Dung dịch Telurit (B1.2) 1 ml
- Dung dịch pyruvat (B1.3) 5 ml
Bằng thao tác vô khuẩn, chia ra các đĩa petri, mỗi đĩa 15 - 20 ml.
B2. Môi trường nước thịt B.H.I.
|
- Pepton |
10g |
|
- Bột óc bê |
12,5g |
|
- Bột tim bê |
5g |
|
- Glucos |
2g |
|
- Natri clorua |
5g |
|
- Natrihydro photphat ( Na2HPO4) |
2,5g |
|
- Nước cất |
1000 ml |
Hoà tan các thành phần trên trong nước sôi. Chỉnh pH 7,6. Chia vào các bình thuỷ tinh mỗi bình từ 10 - 20 m. Hấp 121oC trong 20 phút.
B3. Môi trường nước thịt:
|
- Nước thịt bò |
1000 ml |
|
- Pepton |
10g |
|
- Natri clorua |
5g |
Hoà tan pepton và Natri clorua trong nước thịt, đun sôi. Để nguội, chỉnh pH 7,4 - 7,6. Chia vào các bình thuỷ tinh, mỗi bình từ 10 - 20 ml. Hấp 121oC trong 20 phút.
B4. Môi trường Chapman:
|
- Mannit |
10g |
|
- Bột cao thịt |
1g |
|
- Pepton |
10g |
|
- Natri clorua |
75g |
|
- Thạch |
18 - 20 g |
|
- Đỏ trung tính |
0,025 g |
|
- Nước cất |
1000 ml |
Hoà tan các thành phần trên trong nước đun sôi. Chỉnh pH 7,6. Hấp 121oC trong 15 phút. Chia vào các đĩa petri mỗi đĩa 15 - 20 ml.
B5. Dung dịch ngăm máu đông:
- Natri xitrat 7,8g
- Nước cất 100 ml
Hoà tan trong nước. Chia vào các lọ nhỏ từ 3 - 5 ml. Hấp 121oC trong 15 phút.