Nội dung toàn văn Tiêu chuẩn quốc gia TCVN 8972-1:2011 (EN 12823-1 : 2000) về Thực phẩm - Xác định vitamin A bằng sắc ký lỏng hiệu năng cao – Phần 1: Xác định 13-cis-retinol và tất cả các đồng phân trans-retinol
TIÊU CHUẨN QUỐC GIA
TCVN 8972-1:2011
THỰC PHẨM - XÁC ĐỊNH VITAMIN A BẰNG SẮC KÝ LỎNG HIỆU NĂNG CAO - PHẦN 1: XÁC ĐỊNH 13-CIS-RETINOL VÀ TẤT CẢ CÁC ĐỒNG PHÂN TRANS-RETINOL
Foodstuffs - Determination of vitamin A by high-performance liquid chromatography - Part 1: Measurement of all-trans-retinol and 13-cis-retinol
1. Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp xác định hàm lượng vitamin A trong thực phẩm bằng sắc ký lỏng hiệu năng cao (HPLC). Hàm lượng vitamin A được xác định bằng cách đo b-caroten, 13-cis-retinol và tất cả các đồng phân trans-retinol (all-trans-retinol). Tiêu chuẩn này đề cập đến phép đo all-trans- retinol và 13-cis-retinol.
Dịch chiết thu được sau khi xà phòng hóa có thể được dùng để xác định b-caroten như quy định trong TCVN 8972-2:2011 (EN 12823-2:2000).
2. Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 2625 (ISO 5555), Dầu mỡ động vật và thực vật - Lấy mẫu
TCVN 4851 (ISO 3696), Nước dùng để phân tích trong phòng thí nghiệm - Yêu cầu kỹ thuật và phương pháp thử
3. Nguyên tắc
Retinol được xà phòng hóa bằng dung dịch kali hydroxit trong etanol hoặc trong metanol và được chiết bằng dung môi thích hợp. Sau đó được xác định bằng sắc ký lỏng hiệu năng cao có detector huỳnh quang (F) hoặc detector tử ngoại (UV). Các chất được nhận biết dựa vào thời gian lưu và được xác định bằng phương pháp ngoại chuẩn, dùng diện tích pic hoặc chiều cao pic, xem [1] đến [4].
4. Thuốc thử
Trong quá trình phân tích, chỉ sử dụng các thuốc thử loại tinh khiết phân tích và nước sử dụng ít nhất là loại 1 của TCVN 4851 (ISO 3696), trừ khi có quy định khác.
4.1. Metanol.
4.2. Etanol tuyệt đối, j(C2H5OH)= 100 % thể tích.
4.3. Etanol, j(C2H5OH)= 96 %.
4.4. Natri sulfat, Khan.
4.5. Dung dịch KOH dùng để xà phòng hóa, có các nồng độ khối lượng thích hợp, ví dụ r (KOH)= 50 g/100 ml hoặc 60 g/100 ml, hoặc dung dịch ancol, ví dụ 28 g KOH trong 100 ml hỗn hợp etanol/nước (9 + 1) (tính theo thể tích).
4.6. Chất chống oxi hóa, ví dụ axit ascorbic (AA), natri ascorbat, natri sulfit (Na2S), hydroxytoluen đã butyl hóa (BHT). pyrogallol hoặc hydroquinon.
4.7. Dung môi và dung môi chiết, ví dụ dietyl ete (không chứa peroxit), di-isopropylete, dầu nhẹ (dải sôi từ 40 °C đến 60 °C), n-hexan, butanol hoặc các hỗn hợp thích hợp của chúng.
4.8.Pha động HPLC
Các ví dụ về các hỗn hợp thích hợp (tính theo thể tích) bao gồm:
n-hexan + 2-propanol (98 + 2);
iso-octan + 2-propanol (98,5 + 1,5);
iso-octan + iso-butanol (98 + 2);
n-hexan + n-butanol (98 + 2);
và gradient với 2-propanol + n-heptan, trong khoảng từ (0,5 + 99,5) đến (8,5 + 91,5) trong 12 min.
4.9. Chất chuẩn
4.9.1. Yêu cầu chung
All-trans-retinol (ancol vitamin A all-trans) và 13-cis-retinol có thể thu được dưới một vài dạng khác nhau, từ các nhà cung cấp khác nhau. Vì vậy, cần xác định nồng độ dung dịch hiệu chuẩn bằng đo quang phổ (xem 4.10.4). Nếu sử dụng các este của vitamin A (ví dụ retinyl palmitat hoặc axetat) thì kiểm tra nồng độ sau Khi xà phòng hóa (xem 7.3.1).
CHÚ THÍCH Chú ý về hàm lượng vitamin A của chất chuẩn do các nhà sản xuất khác nhau cung cấp.
4.9.2. All-trans-retinol, ancol vitamin A, M (C20H30O)= 286,5 g/mol, có độ tinh khiết ít nhất 90 %.
4.9.3. Este của vitamin A
4.9.3.1. Retinyl palmitat, vitamin A palmitat, M (C36H60O2)= 524,9 g/mol.
4.9.3.2. Retinyl axetat, vitamin A axetat, M (C22H32O2)= 328,5 g/mol, có độ tinh khiết ít nhất 90 %.
4.9.4. 13-cis-retinol, M(C20H30O)= 286,5 g/mol, có độ tinh khiết ít nhất 60 %, dùng để định tính.
4.10. Dung dịch gốc và dung dịch chuẩn
4.10.1. Dung dịch gốc all-trans-retinol
Cân khoảng 50 mg all-trans-retinol (4.9.2), chính xác đến miligam, cho vào bình định mức một vạch 100 ml, hòa tan trong n-hexan hoặc các dung môi phù hợp khác (4.7) và pha loãng dung dịch đến vạch. Dung dịch gốc chứa khoảng 0,5 mg/ml.
Cách khác, cân khoảng 100 mg retinyl palmitat (4.9.3.1) hoặc 50 mg retinyl axetat (4.9.3.2), chính xác đến miligam, cho vào bình định mức một vạch 100 ml và xử lý tương tự như all-trans-retinol, ngoài ra nồng độ cần được xác định (4.10.4) sau khi xà phòng hóa (7.3.1).
Có thể sử dụng khối lượng và thể tích khác tùy thuộc vào việc tách và định lượng bằng sắc ký.
Bảo quản dung dịch gốc tránh ánh sáng và ở nhiệt độ nhỏ hơn 4 °C.
4.10.2. Dung dịch gốc 13-cis-retinol
Cân khoảng từ 1 mg đến 2 mg 13-cis-retinol (4.9.4), chính xác đến 0,1 mg, cho vào trong bình định mức một vạch 100 ml, hòa tan trong etanol tuyệt đối (4.2), hoặc trong dung môi thích hợp khác rồi pha loãng dung dịch đến vạch. Dung dịch này chứa khoảng từ 10 mg/ml đến 20 mg/ml và được dùng chỉ để nhận biết.
4.10.3. Dung dịch chuẩn all-trans-retinol
Dùng pipet lấy 5 ml dung dịch gốc all-trans-retinol (4.10.1) cho vào bình định mức một vạch 100 ml và pha loãng đến vạch bằng n-hexan (4.7) hoặc các dung môi phù hợp tương thích với pha động. Dùng pipet lấy 5 ml dung dịch này cho vào bình định mức một vạch 50 ml, rồi pha loãng đến vạch bằng cùng một loại dung môi. Dung dịch chuẩn chứa khoảng 2,5 mg/ml. Tiến hành phép thử về độ tinh khiết và nồng độ tinh khiết như quy định trong 4.10.4.
Cách khác, có thể sử dụng các dung dịch gốc retinyl palmiat hoặc retinyl axetat (4.10.1) để chuẩn bị dung dịch chuẩn. Trong trường hợp đó, xà phòng hóa các dung dịch sử dụng các quy định trong 7.3.1. Sau khi chiết và làm bay hơi, hòa tan lại cặn trong n-hexan hoặc dung môi thích hợp và tiến hành như đối với dung dịch gốc của all-trans-retinol.
Bảo vệ dung dịch chuẩn tránh ánh sáng và bảo quản ở nhiệt độ dưới 4 °C.
4.10.4. Phép thử độ tinh khiết và xác định nồng độ
Chuẩn bị dung dịch chuẩn all-trans-retinol trong etanol và đo độ hấp thụ trong cuvet thạch anh có chiều dài đường quang 1 cm, ở bước sóng cực đại từ 325 nm đến 326 nm với cuvet đối chứng chứa etanol.
Tính nồng độ khối lượng của all-trans-retinol, rall-T, bằng microgam trên mililit, theo Công thức (1):
![]() (1)
(1)
Tính nồng độ khối lượng của 13-cis-retinol, r13cis, bằng microgam trên mililit, theo Công thức (2):
![]() (2)
(2)
Trong đó
Aall-T là giá trị độ hấp thụ ở bước sóng cực đại từ 325 nm đến 326 nm;
A13cis là giá trị độ hấp thụ ở bước sóng cực đại 328 nm;
1 830 là giá trị ![]() đối với all-trans-retinol
đã hòa tan trong etanol. Giá trị này có thể thay đổi đáng kể với các dung môi
khác;
đối với all-trans-retinol
đã hòa tan trong etanol. Giá trị này có thể thay đổi đáng kể với các dung môi
khác;
1 686 là giá trị ![]() với 13 cis-retinol đã hòa tan trong
metanol. Giá trị này có thể thay đổi đáng kể với các dung môi khác;
với 13 cis-retinol đã hòa tan trong
metanol. Giá trị này có thể thay đổi đáng kể với các dung môi khác;
P là hệ số hiệu chỉnh về độ tinh khiết của all-trans-retinol hoặc 13-cis-retinol được xác định bằng HPLC và tính được bằng Công thức (3):
P = ![]() (3)
(3)
Trong đó
B là diện tích pic hoặc chiều cao pic của all-trans-retinol hoặc 13-cis-retinol thu được với dung dịch chuẩn (4.10.3);
Bt là tổng diện tích hoặc chiều cao pic từ all-trans-retinol và 13-cis-retinol thu được với dung dịch chuẩn (4.10.3).
Khi dùng các chất chuẩn vitamin A mới mua hoặc đã được bảo quản trong khoảng thời gian dài, cần kiểm tra độ hấp thụ của dung dịch chuẩn của all-trans-retinol (4.10.3), dùng máy đo quang phổ phù hợp đo ở bước sóng cực đại từ 325 nm đến 326 nm.
Để kiểm tra tiếp về các chất chuẩn vitamin A, đo độ hấp thụ của dung dịch chuẩn trong cuvet thạch anh (5.1) ở bước sóng 300 nm, 325 nm, 350 nm và 370 nm với 2-propanol (hoặc dung môi thích hợp khác, xem 4.7) làm đối chứng. Xác định tỷ lệ sau của mỗi bước sóng:
![]() đối với all-trans-retinol
đối với all-trans-retinol
Nếu tỷ lệ này không vượt quá 0,602 (ở bước sóng 300 nm), 0,452 (ở bước sóng 350 nm) và 0,093 (ở bước sóng 370 nm) đối với ancol vitamin A thì chất chuẩn này phù hợp để sử dụng [5], [6].
Đối với retinyl palmitat (4.9.3.1), xác định tỷ lệ của E/E326 ở các bước sóng 300 nm, 350 nm, 370 nm sử dụng 2-propanol (hoặc các dung môi phù hợp khác) làm đối chứng. Nếu tỷ lệ này không vượt quá 0,593 (ở bước sóng 300 nm), 0,537 (ở bước sóng 350 nm) và 0,142 (ở bước sóng 370 nm) thì chất chuẩn này phù hợp để sử dụng [5], [6], [7].
5. Thiết bị, dụng cụ
Sử dụng các thiết bị, dụng cụ của phòng thử nghiệm thông thường và cụ thể như sau:
5.1. Máy đo phổ UV-VIS, có khả năng đo độ hấp thụ ở các bước sóng xác định, với các cuvet thạch anh thích hợp, ví dụ: chiều dài đường quang 1 cm.
5.2. Máy có quay, có nồi cách thủy và bộ phận chân không.
CHÚ THÍCH Nên sử dụng nitơ để giải phóng chân không.
5.3. Hệ thống HPLC, gồm có máy sắc ký lỏng hiệu năng cao, bơm, dụng cụ bơm mẫu, detector UV-VIS hoặc detector huỳnh quang và bộ phân tích dữ liệu.
5.4. Cột HPLC
Các cột pha thường phân tích thích hợp, ví dụ như LiChrospher® Si 601) (5 mm, 250 mm X 4 mm) và LiChrosorb® Si 601) (5 mm, 250 mm X 4 mm và 125 mm X 4 mm). Các tiêu chí đối với các cột phân tích thích hợp là sự phân giải đường nền của all-trans-retinol và 13-cis-retinol.
Có thể sử dụng các loại cột và cỡ hạt khác với quy định trong tiêu chuẩn này. Các điều kiện sắc ký có thể phải được điều chỉnh cho phù hợp đối với các nguyên liệu để đảm bảo cho kết quả tương đương.
5.5. Dụng cụ lọc
Các dụng cụ lọc loại lớn, nhỏ để lọc pha động HPLC và các dung dịch mẫu tương ứng, ví dụ có cỡ lỗ 0,45 mm là thích hợp.
CHÚ THÍCH Việc lọc pha động cũng như dung dịch mẫu thử qua bộ lọc màng trước khi sử dụng hoặc bơm có thể tăng thời gian sử dụng của cột.
5.6. Cột chiết (tùy chọn), ví dụ Extrelut®1)
5.7. Bộ lọc tách pha (tùy chọn).
6. Lấy mẫu
Lấy mẫu theo TCVN 2625 (ISO 5555), nếu thích hợp.
7. Cách tiến hành
7.1. Yêu cầu chung
Vitamin A nhạy với bức xạ UV và các tác nhân oxi hóa (ví dụ, oxi trong không khí). Vì vậy, cần tránh ánh sáng UV (bằng cách dùng dụng cụ thủy tinh màu nâu, lá nhôm hoặc các vật liệu không hấp thụ UV) và oxi (thổi nitơ) khi xử lý vitamin A. Đặc biệt, không khí phía trên dịch lỏng phải được thay thế bằng nitơ trong quá trình xà phòng hóa. Các dung môi phải được làm bay hơi dưới áp suất giảm, dùng máy cô quay chân không (5.2) và ở nhiệt độ không quá 50 °C.
7.2. Chuẩn bị mẫu thử
Đồng hóa mẫu thử. Nghiền thô mẫu bằng dụng cụ nghiền thích hợp và trộn kỹ. Chú ý như làm lạnh sơ bộ mẫu để tránh mẫu tiếp xúc với nhiệt độ cao trong khoảng thời gian dài.
7.3. Chuẩn bị dung dịch mẫu thử
7.3.1 Xà phòng hóa
Xà phòng hóa từ 2 g đến 10 g mẫu thử bằng cách cho đối lưu, tốt nhất dưới dòng nitơ, dùng các lượng thích hợp của metanol (4.1) hoặc etanol (4.3), chất chống oxi hóa (4.6) (tùy chọn) và dung dịch kali hydroxit (4.5). Nếu sử dụng chất chống oxi hóa như axit ascorbic (AA), pyrogallol hoặc hydroxytoluen đã butyl hóa thì chúng phải được thêm vào mẫu trước khi thêm dung dịch kali hydroxit. Có thể bổ sung natri sulfit để phòng ngừa ảnh hưởng của các kim loại dạng vết.
Các ví dụ về tỷ lệ các thuốc thử phù hợp được nêu trong Bảng 1.
Bảng 1 - Tỷ lệ thích hợp của các thuốc thử
|
Khối lượng mẫu |
Ancol |
Chất chống oxi hóa |
Kali hydroxit |
|
2 g đến 5 g |
50 ml metanol |
0,25 g AA |
5 ml dung dịch 50 g/100 ml |
|
5 g đến 10 g |
100 ml etanol |
1 g AA + 0,04 g Na2S |
20 m dung dịch 60 g/100 ml |
|
10 g đến 20 g |
150 ml etanol |
1 g AA |
50 ml dung dịch 60 g/100 ml |
Thông thường, thời gian xà phòng hóa là từ 15 min đến 45 min ở nhiệt độ từ 80 °C đến 100 °C. Quá trình xà phòng hóa có thể cũng được tiến hành qua đêm ở nhiệt độ phòng (khoảng 16 h) trong các điều kiện tương đương.
Nếu sau khi xà phòng hóa và làm nguội, vẫn còn chất béo hoặc dầu thực vật trên bề mặt hỗn hợp xà phòng hóa, thì bổ sung kali hydroxit trong etanol và kéo dài thời gian xà phòng hóa.
7.3.2. Chiết
Để tránh tạo nhũ, nên bổ sung một lượng nước vào dung dịch mẫu đã xà phòng hóa sao cho tỷ lệ của ancol với nước có trong dung dịch tạo thành là 1:1.
Chiết retinol ra khỏi dung dịch mẫu đã xà phóng hóa bằng dung môi thích hợp hoặc hỗn hợp dung môi thích hợp khác (4.7) và lặp lại quy trình từ 3 lần đến 4 lần với các thể tích từ 50 ml đến 150 ml. Rửa các dịch chiết hỗn hợp cho đến trung tính bằng nước (từ 2 lần đến 4 lần, mỗi lần từ 50 ml đến 150 ml). Việc chiết có thể cũng được thực hiện bằng kỹ thuật chiết lỏng/lỏng có hỗ trợ pha rắn (ví dụ Extrelut®2)) khi hàm lượng retinol không quá thấp và hàm lượng chất béo của mẫu nhỏ hơn 10 % [1].
7.3.3. Làm bay hơi
Cho bay hơi dịch chiết bằng máy cô quay (5.2) dưới áp suất giảm ở nhiệt độ không quá 50 °C. Loại bỏ hết nước bằng cách dùng natri sulfat (4.4) hoặc bằng cách chưng cất đồng sôi với etanol tuyệt đối (4.2), hoặc dùng giấy lọc tách pha (5.5).
7.3.4. Pha loãng
Hòa tan lại cặn, tốt nhất là dùng pha động (4.8), hoặc dung môi thích hợp khác dùng cho HPLC để thu được nồng độ thích hợp để bơm lên cột HPLC (5.4). Đây là dung dịch mẫu thử.
7.4. Chuẩn bị dung dịch hiệu chuẩn
Dùng các dung dịch chuẩn (4.10.3), để chuẩn bị các dung dịch hiệu chuẩn dùng cho HPLC, sử dụng các dung môi thích hợp bao trùm dải nồng độ cần phân tích.
7.5. Nhận biết và kiểm tra độ tinh khiết
Nhận biết all-trans-retinol và 13-cis-retinol bằng cách so sánh thời gian lưu từ sắc đồ của mẫu với thời gian lưu thu được từ các chất chuẩn trong cùng điều kiện sắc ký. Việc nhận biết pic có thể được thực hiện bằng cách bổ sung các chất chuẩn vào dung dịch mẫu thử.
CHÚ THÍCH 1 Việc tách và định lượng cho thấy là thỏa mãn nếu tuân thủ các điều kiện sắc ký sau đây (xem thêm Hình A.1). Đối với các hệ thống HPLC thay thế, xem Bảng C.1.
Pha tĩnh: Merck LiChrosorb®Si60,5 mm
Kích thước cột: 250 mm x 4 mm
Pha động: n-hexan + n-butanol (98 + 2) (thể tích)
Tốc độ dòng: 2ml/min
Thể tích bơm: 50 ml
Detector: huỳnh quang: bước sóng kích thích 325 nm, bước sóng phát xạ: 475 nm
tử ngoại (UV): bước sóng 325 nm.
Kiểm tra độ tinh khiết của các chất chuẩn của all-trans-retinol và 13-cis-retinol bằng cách bơm một thể tích thích hợp (ví dụ: 20 ml) của các dung dịch chuẩn (4.10.3) chứa khoảng 10 mg all-trans-retinol hoặc 13-cis-retinol trên mililit vào hệ thống HPLC. Tích phân diện tích pic hoặc chiều cao pic của all-trans-retinol, 13-cis-retinol và hiệu chỉnh nồng độ khối lượng của dung dịch chuẩn all-trans-retinol, nếu cần.
CHÚ THÍCH 2 Các chất chuẩn của all-trans-retinol mới được chuẩn bị (4.10.3) thường không chứa bất kỳ 13-cis-retinol hoặc các pic tạp nhiễu nào khác. Este của vitamin A (retinylpalmitat hoặc axetat) có thể chứa một lượng nhỏ 13-cis-retinol sau khi xà phòng hóa.
7.6. Xác định
Bơm các thể tích thích hợp (ví dụ 20 ml) của dung dịch chuẩn (4.10.3) và dung dịch thử (7.3.4) vào hệ thống HPLC (5.3). Tiến hành xác định bằng phương pháp ngoại chuẩn, tích phân diện tích pic hoặc xác định chiều cao pic thu được đối với các dung dịch thử và so sánh các kết quả với các giá trị tương ứng đối với chất chuẩn có thời gian lưu tương tự, hoặc dựng đường chuẩn.
Bơm các thể tích bằng nhau của dung dịch mẫu thử và các dung dịch chuẩn đã được chuẩn bị phù hợp với hệ thống HPLC, hoặc bù bằng hệ số tương ứng trong phép tính các kết quả (Điều 8). Kiểm tra độ tuyến tính của đường chuẩn.
CHÚ THÍCH Có thể sử dụng các quy trình nội chuẩn nếu các phép thử về độ thu hồi tương ứng được chứng minh phù hợp. Ngoài ra các hợp chất thích hợp khác có thể được bổ sung vào dung dịch thử trước khi bơm lên cột HPLC để định lượng [6]
7.7. Số lần xác định
Tiến hành ít nhất hai lần xác định độc lập.
8. Tính kết quả
Dựa vào phép tính theo đường chuẩn trên dải tuyến tính hoặc theo quy trình đã đơn giản hóa.
Tính nồng độ khối lượng của all-trans-retinol, rall-trans, bằng miligam trên 100 g (mg/100 g), theo Công thức (4):
![]()
Trong đó:
As là diện tích pic hoặc chiều cao pic đối với all-trans-retinol thu được trong dung dịch mẫu thử (7.3.4), tính bằng đơn vị diện tích hoặc đơn vị chiều cao;
Call-T là nồng độ của all-trans-retinol đo được bằng detector UV (4.10.4) trong dung dịch chuẩn (7.4), tính bằng microgam trên mililit (ng/ml);
Vs là tổng thể tích của dung dịch mẫu thử (7.3.4), tính bằng mililit (ml);
Vst là thể tích bơm của dung dịch chuẩn (7.4), tính bằng microlit (ml);
100 là hệ số để tính nồng độ khối lượng trên 100 g;
Aall-T là diện tích hoặc chiều cao pic đối với tất cả all-trans-retinol thu được bằng dung dịch chuẩn (7.4), tính bằng đơn vị diện tích hoặc đơn vị chiều cao;
m là khối lượng của phần mẫu thử, tính bằng gam (g);
Vis là thể tích bơm của dung dịch mẫu thử, tính bằng microlit (ml);
1 000 là hệ số chuyển đổi từ microgam sang miligam.
Tính nồng độ khối lượng của 13 cis-retinol, r13-cis, bằng miligam trên 100 g (mg/100 g), theo Công thức (5):
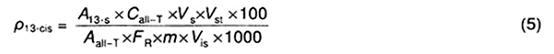
Trong đó:
A13-s là diện tích pic hoặc chiều cao pic đối với 13-cis-retinol thu được bằng dung dịch mẫu thử (7.3.4), tính bằng các đơn vị diện tích hoặc chiều cao;
Call-T là nồng độ của all-trans-retinol đo được bằng detector UV (4.10.4) trong dung dịch chuẩn (7.4), tính bằng microgam trên mililit (mg/ml);
Vs là tổng thể tích của dung dịch thử (7.3.4), tính bằng mililit (ml);
Vst là thể tích bơm dung dịch chuẩn (7.4), tính bằng microlit (ml);
100 là hệ số để tính nồng độ khối lượng trên 100 g;
Aall-T là diện tích hoặc chiều cao pic đối với tất cả các đồng phân trans-retinol thu được bằng dung dịch chuẩn (7.4), tính bằng đơn vị diện tích hoặc đơn vị chiều cao;
m là khối lượng của phần mẫu thử, tính bằng gam (g);
Vis là thể tích bơm của dung dịch mẫu thử (7.3.4), tính bằng microlit (ml);
1 000 là hệ số chuyển đổi từ microgam sang miligam;
FR là hệ số đáp ứng của 13-cis-retinol đến all-trans-retinol được đánh giá bằng HPLC, dùng dung dịch chuẩn đã biết nồng độ, sử dụng Công thức 6:

Trong đó:
B13cis là diện tích pic hoặc chiều cao pic thu được đối với dung dịch chuẩn 13-cis-retinol;
Ball-T là diện tích pic hoặc chiều cao pic thu được đối với dung dịch chuẩn all-trans-retinol;
C13cis là nồng độ khối lượng của dung dịch chuẩn 13-cis-retinol;
Call-T là nồng độ khối lượng của dung dịch chuẩn all-trans-retinol.
9. Độ chụm
9.1. Yêu cầu chung
Các chi tiết của phép thử liên phòng thử nghiệm về độ chụm của phương pháp được nêu trong Phụ lục B. Các giá trị thu được từ phép thử liên phòng thử nghiệm này có thể không áp dụng cho các dải nồng độ và chất nền khác với các dải nồng độ và chất nền đã nêu trong Phụ lục B.
9.2.Độ lặp lại
Chênh lệch tuyệt đối giữa các kết quả của hai phép thử đơn lẻ thu được khi sử dụng cùng phương pháp trên vật liệu thử giống hệt nhau trong cùng một phòng thử nghiệm, do một người thực hiện, sử dụng cùng thiết bị, thực hiện trong một khoảng thời gian ngắn, không quá 5 % các trường hợp lớn hơn giới hạn lặp lại r.
Các giá trị là:
|
Margarin |
all-trans-retinol |
|
mg/100g |
r = 78,4 |
mg/100g |
|
|
13-cis-retinol |
|
mg/100g |
r =8,4 |
mg/100g |
|
Sữa bột |
all-trans-retinol |
|
mg/100g |
r =39,2 |
mg/100g |
|
|
13-cis-retinol |
|
mg/100g |
r =4,2 |
mg/100g |
9.3. Độ tái lập
Chênh lệch tuyệt đối giữa các kết quả của hai phép thử đơn lẻ, thu được khi sử dụng cùng phương pháp, tiến hành thử trên vật liệu giống nhau, do hai phòng thử nghiệm thực hiện, không quá 5% các trường hợp lớn giới hạn tái lập R.
|
Các giá trị là: |
|
|
|
|
|
|
Margarin |
all-trans-retinol |
|
mg/100g |
R = 204,4 |
mg/100g |
|
|
13-cis-retinol |
|
mg/100g |
R = 33,6 |
mg/100g |
|
Sữa bột |
all-trans-retinol |
|
mg/100g |
R = 61,6 |
mg/100g |
|
|
13-cis-retinol |
|
mg/100g |
R =20,2 |
mg/100g |
10. Báo cáo thử nghiệm
Báo cáo thử nghiệm ít nhất phải bao gồm các thông tin sau đây:
- mọi thông tin cần thiết để nhận biết đầy đủ về mẫu thử;
- viện dẫn tiêu chuẩn này hoặc phương pháp thử đã sử dụng;
- các kết quả và các đơn vị biểu thị kết quả;
- ngày và quy trình lấy mẫu (nếu biết);
- ngày nhận mẫu:
- ngày thử nghiệm;
- các điểm đặc biệt quan sát được trong khi tiến hành thử nghiệm;
- mọi chi tiết thao tác không được quy định trong tiêu chuẩn này hoặc những điều được coi là tùy chọn có thể ảnh hưởng đến kết quả.
PHỤ LỤC A
(tham khảo)
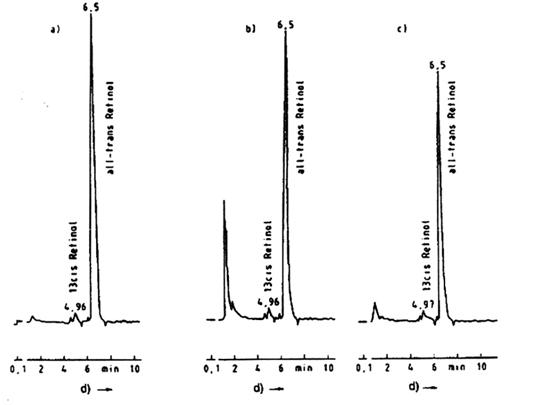
CÁC VÍ DỤ VỀ SẮC ĐỒ HPLC
|
d) |
Thời gian; |
|
Cột: |
Merck LiChrosorb®Si 60 (5 mm); |
|
Kích thước cột: |
250 mm X 4 mm; |
|
Pha động |
n-hexan + n-butanol (98 + 2) (thể tích); |
|
Tốc độ dòng: |
2 ml/min; |
|
Detector: |
Huỳnh quang, bước sóng kích thích: 325 nm, bước sóng phát xạ: 475 nm. |
Hình A.1 - Sắc đồ HPLC của các chất chuẩn vitamin A (a), vitamin A trong margarin (b) và sữa bột (c)
PHỤ LỤC B
(tham khảo)
DỮ LIỆU VỀ ĐỘ CHỤM
Hướng dẫn phù hợp với các nghiên cứu chứng nhận EU MAT, các thông số cho trong Bảng B.1 đã được xác định trong một phép thử liên phòng thử nghiệm [3]. Nghiên cứu này do Viện nghiên cứu thực phẩm, Norwich, Vương quốc Anh tổ chức.
Bảng B.1 - Kết quả thử liên phòng thử nghiệm
|
Mẫu |
Margarin (CRM 122)* |
Bột sữa (CRM 421)* |
||
|
All-trans-retinol |
13-cis-retinol |
All-trans-retinol |
13-cis-retinol |
|
|
Năm tiến hành phép thử liên phòng thử nghiệm |
1994 |
1994 |
1994 |
1994 |
|
Số lượng phòng thử nghiệm |
9 |
5 |
8 |
5 |
|
Số lượng mẫu |
2 |
2 |
2 |
2 |
|
Số lượng các phòng thử nghiệm còn lại sau khi trừ ngoại lệ |
9 |
5 |
6 |
5 |
|
Số lượng các phòng thử nghiệm ngoại lệ |
0 |
0 |
2 |
0 |
|
Số lượng các kết quả được chấp nhận |
45 |
25 |
40 |
21 |
|
Giá trị trung bình, |
729 |
39 |
653 |
30 |
|
Độ lệch chuẩn lặp lại, sr mg/100 g |
28 |
3 |
14 |
1,5 |
|
Độ lệch chuẩn tương đối lặp lại, RSDr % |
3,8 |
7,7 |
2,1 |
5.0 |
|
Giới hạn lặp lại, r, mg /100 g |
78,4 |
8,4 |
39,2 |
4,2 |
|
Độ lệch chuẩn tái lập. sR, mg /100 g |
73 |
12 |
22 |
7,2 |
|
Độ lệch chuẩn tương đối tái lập, RSDR, % |
10,0 |
30,8 |
3,4 |
24,0 |
|
Giới hạn tái lập, R, mg /100 g |
204,4 |
33,6 |
61,6 |
20,2 |
|
* CRM= chất chuẩn đã được chứng nhận. |
||||
PHỤ LỤC C
(tham khảo)
HỆ THỐNG HPLC THAY THẾ
Việc tách, định lượng all-trans-retinol và 13-cis-retinol cho thấy thỏa mãn nếu sử dụng [3] các điều kiện sắc ký trong Bảng C.1 dưới đây:
Bảng C.1 - Các điều kiện sắc ký
|
Cột (cỡ hạt) |
Kích thước (dài X đường kính) |
Pha động (V+V) |
Phát hiện (l/nm) |
|
LiChrospher®Si 60 (5 mm) |
250 mm X 4 mm |
n-hexan + 2propanol (98 + 2) |
F (325/480) |
|
LiChrospher®Si 60 (5 mm) |
250 mm X 4 mm |
n-hexan + n-butanol (98 + 2) |
F (325/475) |
|
LiChrosorb®Si 60 (5 mm) |
250 mm X 4 mm |
lso-propanol: n-heptan, gradient: từ (0,5 + 99,5) đến (8,5 + 91,5) trong 12 min |
UV 325 |
THƯ MỤC TÀI LIỆU THAM KHẢO
[1] Bourgeois, C.F. and Ciba, N., 1988. Disposal cartridge extraction of retinol and alpha-tocopherol from fatty samples. J.A.0.A.C 71 (I), 12-15.
[2] Leth, T., 1993. Vitamin A in Danish pig, calf and ox liver. J. Food Composition & Analysis 6, 3-9.
[3] Finglas, P.M., van den Berg, H. & de Froidmont-Gortz, I., 1997. The certification of the mass fractions of vitamins in three reference materials: margarine (CRM 122), milk powder (CRM 421), and lyophilized Brussels sprouts (CRM 431). EUR-Report 18039, Commission of the European Union, Luxembourg.
[4] Untersuchung von Lebensmitteln: Bestimmung von Vitamin A in diätetischen Lebensmitteln L 49.00-3, Mai 1985 (Food Analysis: Determination of vitamin A in dietetic foodstuffs L 49.00-3, 1985-05) in: Amtliche Sammlung von Untersuchungsverfahren nach Q 35 LMBG: Verfahren zur Probenahme und Untersuchung von Lebensmitteln, Tabakerzeugnissen, kosmetischen Mitteln und Bedarfsgegenständen/Bundesgesundheitsamt
(In: Collection of official methods under article 35 of the German Federal Foods Act; Methods of sampling and analysis of foods, tobacco Products, cosmetics and commodity goods/Federal Health Office) Loseblattausgabe, Stand Februar 1996 Bd. I (Loose leaf edition, as of 1996-02 Vol. i.) Berlin, Köln: Beuth Verlag GmbH.
[5] Takashima, Y. et al., 1979. Stability of retinol analogs. Chern. Pharm. Bull. 27,1553.
[6] Bolliger, M.R. et al., 1977. The monograph of vitamin A in the European Pharmacopoeia. Pharm. Acta. Helv. 52 (8), 161-174.
[7] Arens, M. and Gertz, Chr., 1996. Gehaltsbestimmung von Vitamin A-Standardsubstanzen - Deutsche Einheitsmethoden zur Untersuchung von Fetten, Fettprodukten, Tensiden und verwandten Stoffen, 124. Mitt.; (Determination of vitamin A content in Standard substances - German methods for analysis of fats, fat products, tensids and related products, 124. ann) Fett/Lipid, VCH Verlag. Weinheim, 98, Nr. 5, S. 185-187.
1) LiChrospher® Si 60, LiChrosorb® Si 60 và Extrelut® là các ví dụ về các sản phẩm phù hợp bán sẵn. Thông tin này tạo thuận tiện cho người sử dụng tiêu chuẩn và tiêu chuẩn này không ấn định phải sử dụng chúng.


